铁死亡(Ferroptosis)在甲状腺癌治疗中的潜力:一种新兴的治疗策略
 学术前沿官方号
学术前沿官方号随着对甲状腺癌病理机制研究的深入,科学家们发现了一种新的程序性细胞死亡模式——铁死亡(ferroptosis),它在甲状腺癌的预后和进展中扮演着重要角色。近年来,铁死亡相关基因(ferroptosis-related genes,FRGs)在甲状腺癌的诊断中显示出了其重要性。本文综述了甲状腺癌的病理和临床特征,并深入探讨了铁死亡与甲状腺癌的基础和功能之间的关系,旨在为甲状腺癌的诊断和治疗提供新的思路和方法。通过对铁死亡在甲状腺癌中的作用进行细致的分析,我们发现了一系列的生物标志物和潜在的治疗靶点,这些发现为开发针对铁死亡的新型治疗策略提供了科学依据,有望为甲状腺癌患者带来更为有效的治疗方案。
甲状腺癌概述
1.甲状腺癌的组织学亚型
甲状腺癌的组织学亚型包括乳头状癌、滤泡状癌、髓样癌和未分化癌。其中,乳头状癌是最常见的类型,占甲状腺癌的80%以上。髓样癌占约10%,而未分化癌(UC)预后较差,发展迅速,早期即可发生颈部淋巴结转移,常通过血液供应发生远处转移,致死率高。
2.甲状腺癌的分期
根据美国癌症研究协会(AARC)的甲状腺癌分期标准,分期指标包括年龄和肿瘤浸润程度。55岁是影响分期的关键因素,甲状腺癌的进展分为四个阶段(I至IV)。随着癌症从I期发展到IV期,患者的生存率会降低。I期和II期的主要特点是肿瘤细胞局限于甲状腺内,但肿瘤的最大直径不同。III期的主要特点是肿瘤细胞扩散到甲状腺外并发生侵袭。IV期定义为远处转移(例如肺部、骨骼和其他器官,肿瘤也可能围绕颈动脉发生)。
3.诊断和治疗
近年来,随着甲状腺癌超声成像技术的不断改进,实验室诊断中各种指标的敏感性不断提高,如甲状腺球蛋白抗体(TgAb)、甲状腺刺激激素受体抗体(TRAb)等。此外,卷积神经网络(CNNs)和降维技术(DRTs)、分类正则化的均匀流形近似和投影(CReUMAP)嵌入技术在判断甲状腺结节方面具有高准确性,从而提高了甲状腺癌的筛查率,并导致了发病率及诊断率的明显上升趋势。甲状腺癌的治疗方法多种多样,包括手术、放射性核素治疗、促甲状腺激素(TSH)抑制治疗和外照射治疗,其中手术是主要的治疗方法,大多数患者在手术后预后良好。尽管大多数甲状腺癌是惰性肿瘤,但也容易发生颈部淋巴结转移。约30%-80%的乳头状甲状腺癌患者存在颈部淋巴结转移,其中中央区(VI区)淋巴结最容易转移,可占所有患者的约33%。晚期甲状腺癌患者可以尝试使用新辅助疗法等措施。
甲状腺癌中的铁死亡
铁死亡是一种与脂质过氧化相关的铁依赖性细胞死亡方式,在多种癌症,包括甲状腺癌的进展中发挥作用。研究发现,铁死亡相关基因在甲状腺癌中的表达与患者的预后密切相关,且铁死亡诱导剂对甲状腺癌细胞的活性有显著影响。
1.甲状腺癌中的基于铁死亡的预后特征
在甲状腺癌中,基于铁死亡相关基因(FRGs)的表达数据,研究者从癌症基因组图谱(TCGA)数据集中识别出两个亚型,其中与铁死亡正相关的FRGs在第二亚型中的比例更高。基于TCGA的甲状腺癌数据集,发现包含TXNRD1、TFRC、TF、SRXN1、PGD、ISCU、DRD4、DPP4、CDKN2A和ANGPTL7的10个FRGs特征签名是整体生存率(OS)和无病生存率(DFS)的独立预后因素。此外,AKR1C3的高表达和BID、FBXW7、GPX4、MAP3K5的低表达水平与甲状腺癌患者的不利预后正相关,这些基因也是独立的预后因素。
2.铁死亡在甲状腺癌进展中的作用
铁死亡在甲状腺癌的进展中扮演着关键角色,近年来的研究主要集中在甲状腺癌组织与正常组织之间中间激素水平和受体活性的差异表达上。通过对来自癌症基因组图谱(TCGA)的甲状腺癌数据集进行分析,发现与相邻正常组织相比,甲状腺肿瘤组织中有176个基因表达差异,这些基因在基因本体(GO)分析中富集在甲状腺激素、脂质代谢和受体激活等方面,在京都基因与基因组百科全书(KEGG)分析中富集在甲状腺激素合成和过氧化物酶体增殖物激活受体(PPAR)信号通路中。此外,FRGs的多态性与甲状腺癌风险有关,其中BCL3和ALOX5AP的某些多态性与甲状腺癌风险的增加显著相关。与正常甲状腺滤泡上皮细胞相比,甲状腺癌细胞FTC133和TPC-1中cicr_0067934表达上调,其沉默可诱导细胞凋亡并抑制甲状腺癌细胞的增殖,同时增加铁死亡标志物的水平,包括Fe2+、铁和活性氧(ROS)。从机制上讲,cicr_0067934通过吸附miR-545-3p并上调下游的SLC7A11来抑制甲状腺癌细胞的铁死亡。此外,从荷花中提取的双苯基异喹啉生物碱类化合物neferine能够通过调节Nrf2-HO-1-NQO1信号通路抑制甲状腺癌细胞的活力,并诱导细胞凋亡和铁死亡。脂肪质量和肥胖相关蛋白(FTO)是m6A的明确去甲基化酶,其敲低能够增强整个转录组中3'UTR和5'UTR的m6A水平。最近的研究表明,FTO在乳头状甲状腺肿瘤组织中表达下降,并通过以m6A依赖的方式下调SLC7A11来抑制乳头状甲状腺肿瘤的发展。值得注意的是,FTO/SLC7A11轴也能以一种非m6A依赖的方式抑制甲状腺癌的进展。
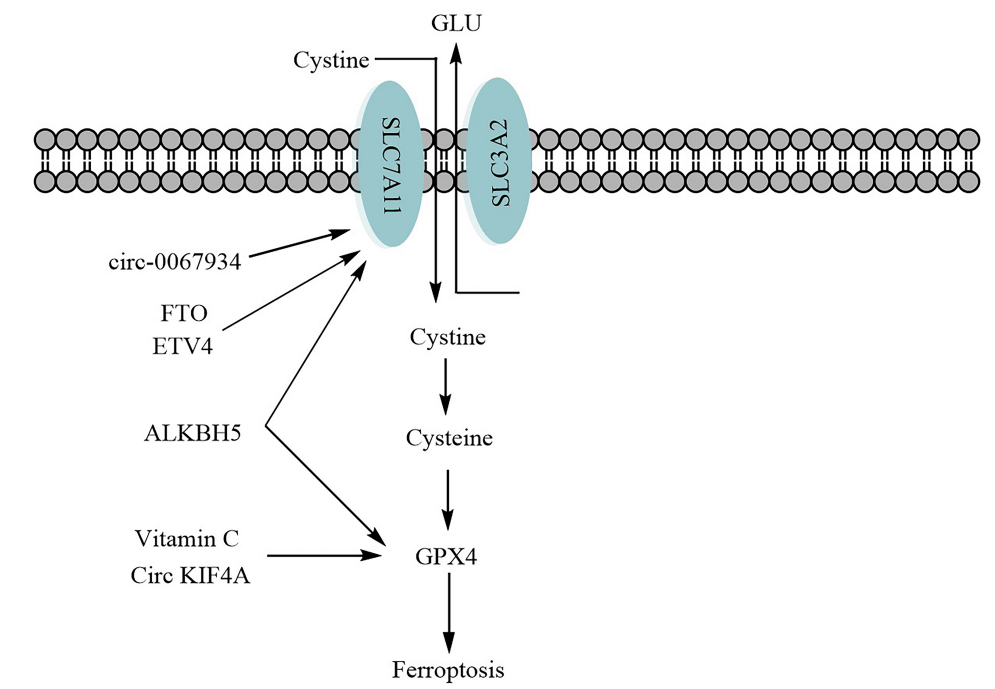
以铁死亡为靶点增强抗甲状腺癌作用的可能机制
FTO,脂肪质量和肥胖相关蛋白;ETV4,变体4;Circ KIF4A,KIF4A的循环转录本;SLC7A11,溶质载体家族7成员11;SLC3A2,溶质载体家族3成员2;GLU,谷胱甘肽。
总结与展望
铁死亡作为一种调控性细胞死亡方式,近年来研究发现其与多种恶性肿瘤的发病机制关系密切,参与的信号通路在恶性肿瘤的发生发展中起着重要作用。尽管甲状腺癌的恶性程度通常不高,但其发病率逐年上升,且趋于年轻化。本综述总结了铁死亡在甲状腺癌细胞发展中的参与情况,并探讨了铁死亡相关基因的作用机制。目前虽未有针对铁死亡的临床应用药物或技术,但预计未来对铁死亡机制的研究会促进靶向药物的开发,为晚期甲状腺癌患者治疗带来重大突破。然而,甲状腺癌细胞对铁死亡的抵抗机制尚未完全阐明,特别是在肿瘤免疫方面,需要进一步研究。
参考文献
[1]Rongyi Hu,Zhizhou Shi,Jie Yang,Yanxin Ren,Xiaojiang Li.Anti-Ferroptosis:A Promising Therapeutic Method for Thyroid Cancer.Front.Biosci.(Landmark Ed)2024;29(2):77.https://doi.org/10.31083/j.fbl2902077
原创文章:方舟健客版权所有,未经许可不得转载。