一年两次!长效HIV创新药在中国申报上市,高耐药患者或将迎来治疗新选择
 健客医生官方号
健客医生官方号9月23日,国家药监局药品审评中心官网公示,受理了吉利德科学递交的5.1类新药lenacapavir(音译:来那帕韦)片剂的上市申请。
据悉,这是一种基于衣壳抑制剂的人体免疫缺陷病毒(HIV)的治疗方案,此“first-in-class”药物向HIV患者提供了一种新的、一年两次的治疗选择。
截图来源:CDE官网
HIV 衣壳抑制剂获FDA 批准上市
当地时间2022年12月22日,美国FDA批准lenacapavir上市,用于联合其他抗逆转录病毒药物(ARV)治疗多重耐药(MDR)人类免疫缺陷病毒(HIV)感染的成人患者。
该批准是得到了2/3期“CAPELLA”临床试验数据的支持,研究评估了lenacapavir与优化的背景方案联合应用于多重耐药HIV患者的疗效与安全性。
该试验入组了72例对抗病毒药物多重耐药的HIV感染者,随机分为两组,一组以双盲试验接受lenacapavir和安慰剂,另外一组以开放标签接受lenacapavir,试验的主要终点是在治疗最初的14天内与基线相比达到一定水平病毒减少的患者比例。
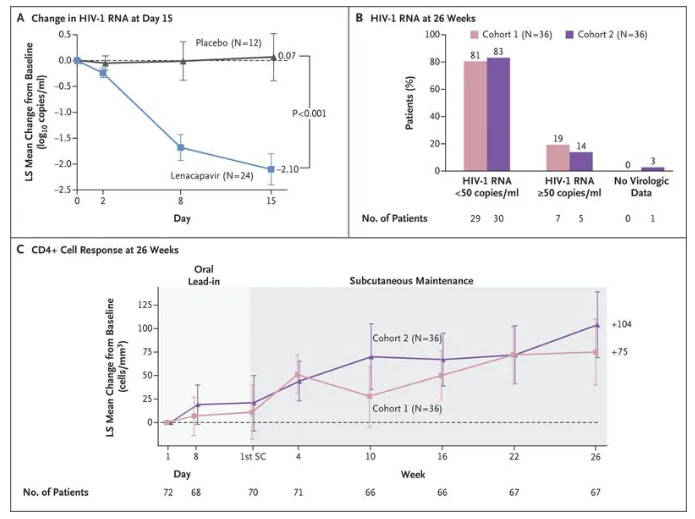
结果发现,接受lenacapavir治疗的患者中有88%(n=21/24)的人实现了病毒的减少,而接受安慰剂治疗的患者中只有17%(n=2/12)的人实现了病毒的减少。
让人惊喜的是,在lenacapavir联合其他抗病毒治疗的第一组试验中,26周后仍然有81%参与者实现了HIV RNA 抑制,其体内的HIV病毒载量水平低至检测不到的水平(<50拷贝/毫升)。52周后,83%的参与者继续有HIV RNA抑制,而且,受试者的CD4阳性细胞计数平均增加82个细胞/微升。
在安全性方面,lenacapavir的耐受性良好,没有观察到与试验中的其他药物相关的严重不良事件,在试验观察的14天内,没有因不良事件停药。
一年两次,对高耐药性 HIV 患者有效
据联合国艾滋病规划署(UNAIDS)公布的流行病学数据,截至2022年,全球共有约3900万艾滋病毒感染者,其中约2980万人正在接受抗逆转录病毒治疗。
由于晚发现、用药依从性不佳和耐药毒株流行等问题,每年仍然有相当多的感染者因艾滋病相关并发症死亡。
传统抗HIV抗病毒药物只是作用于病毒复制的一个阶段,创新药lenacapavir是作用于病毒生命周期的多个阶段,通过与衣壳蛋白单体结合,让生成的病毒衣壳成为功能失常的“伪劣产品”。
该药的创新优势满足了两种HIV感染人群的用药需求:
一是对于多重耐药HIV感染者的治疗诉求;
二是极大提高了便利性,简化了给药次数(每年仅需要给药两次),适用于难以承受复杂治疗方案的HIV感染者。
值得一提的是,早在2019年5月,FDA授予lenacapavir突破性疗法认定。2021年,lenacapavir曾入选猎药人(drughunter)网站公布年度小分子榜单,且位列该榜单第一位。

据悉,已经在美国和欧美上市的lenacapavir分为片剂和注射剂,片剂用于长效lenacapavir注射液给药前的口服方案。
“lenacapavir现在是FDA批准每年两次治疗多重耐药HIV患者的药物,可能会在HIV流行结束工作中起到重要的推动作用。”吉利德科学公司董事长兼首席执行官Daniel O’Day说道。
我们也期待lenacapavir早日进入中国市场,为中国HIV感染者提供一种全新的长效药物选择。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved Sep 23,2023. From https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2]Sunlenca®(lenacapavir)Receives FDA Approval as a First-in-Class,Twice-Yearly Treatment Option for People Living With Multi-Drug Resistant HIV from https://www.gilead.com/news-and-press/press-room/press-releases/2022/12/sunlenca-lenacapavir-receives-fda-approval-as-a-firstinclass-twiceyearly-treatment-option-for-people-living-with-multidrug-resistant-hiv
[3]联合国艾滋病规划署最新发布《2023全球艾滋病防治进展报告 – 终结艾滋病之路》
原创文章:方舟健客版权所有,未经许可不得转载。