本周「8.2-8.9」资讯:替尔泊肽三期试验HFpEF心衰患者获益显著|CEPI&WHO呼吁全面研究病原体家族以应对下一次大流行|诺华肾病新药获FDA批准
 医周动态官方号
医周动态官方号1. 礼来替尔泊肽三期试验告捷:肥胖心衰患者相关事件风险降低38%
本周,礼来公司宣布其抗肥胖药物替尔泊肽(Tirzepatide)在一项关键性的3期临床试验中展示了显著的心血管获益。这项名为SUMMIT的研究首次证实,替尔泊肽不仅能帮助肥胖患者减重,还能显著降低心衰合并肥胖患者的心血管风险。研究数据显示,替尔泊肽能够将心力衰竭相关事件的风险(包括心力衰竭急诊就诊、住院,口服利尿剂强化治疗或心血管死亡)降低38%,相比安慰剂效果显著。
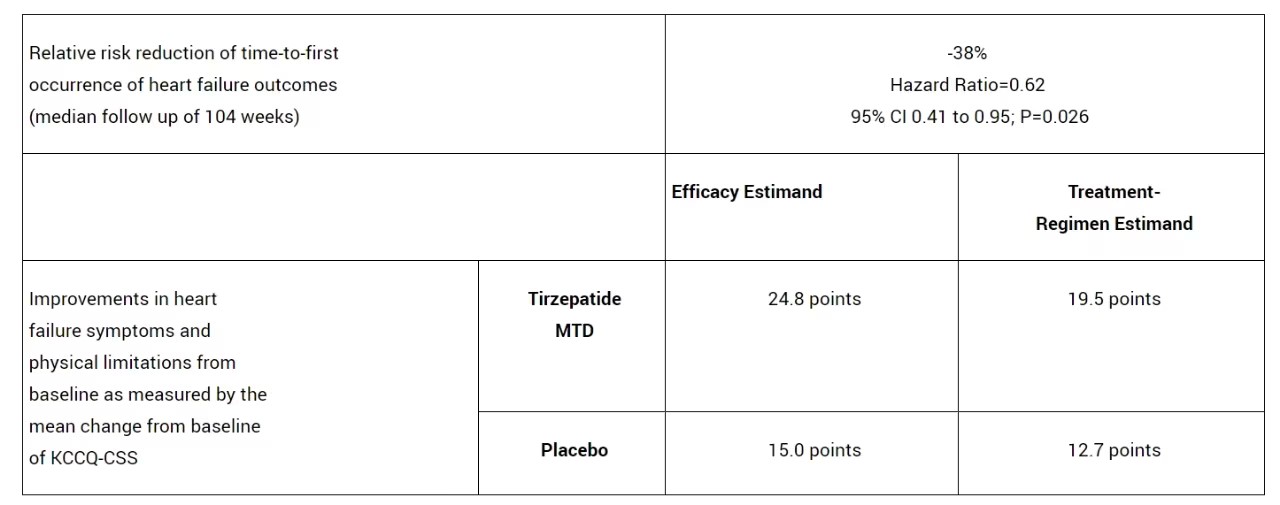
表1 主要终点结果
这项研究主要针对射血分数保留的心衰(HFpEF)伴肥胖患者。HFpEF约占所有心衰病例的一半,而在美国,近60%的HFpEF患者同时伴有肥胖。然而,针对这类患者的有效治疗选择依然有限。此次研究的成功标志着替尔泊肽有望填补这一治疗空白,为大量患者带来新的希望。
除了显著的心衰风险降低,替尔泊肽还在其他关键指标上表现出色。研究显示,在为期52周的治疗中,替尔泊肽治疗组的患者平均体重减少了15.7%,而安慰剂组仅为2.2%。此外,替尔泊肽还显著改善了患者的心衰症状和身体活动能力,尤其是在6分钟步行测试中显示出明显进步,并且显著降低了炎症标志物高敏C反应蛋白(hsCRP)水平。
礼来计划在今年晚些时候将这项研究结果提交给监管机构,以期为替尔泊肽在肥胖合并HFpEF患者中的使用获得进一步批准。这一成功也使礼来在与诺和诺德的竞争中占据了一席之地,后者的抗肥胖药——司美格鲁肽此前在类似人群中也显示出一定的心血管益处。
目前,礼来正在进行多项替尔泊肽的心血管研究,旨在验证其在心血管疾病患者中的预防作用。特别是在2型糖尿病患者中的一项研究预计将在明年获得结果,而针对肥胖患者的另一项研究结果预计将在2027年公布。
2. CEPI与WHO共同呼吁:全面研究病原体家族以应对下一次大流行
世界卫生组织(WHO)和流行病防范创新联盟(CEPI)近日在2024年全球大流行病准备峰会上呼吁各国研究人员和政府加强和加速全球研究,以应对下一次大流行病。此次峰会在巴西里约热内卢举行,重点讨论了通过广泛研究病原体家族来提高大流行病的防范能力。

图片来源:https://cepi.net/global-summit-reinvigorates-efforts-prepare-future-pandemics
WHO发布的R&D Blueprint for Epidemics报告强调了扩展研究范围的重要性,不仅关注个别病原体,还应覆盖所有可能感染人类的病原体家族。该报告建议使用原型病原体作为指南,建立整个病原体家族的知识基础,旨在快速适应新出现的威胁,加速对病原体传播和感染机制以及免疫系统反应的研究。
报告作者形象地比喻道,科学家们如同在街上寻找遗失的钥匙(下一次大流行病的病原体),街灯照亮的区域代表已知的具有大流行潜力的病原体。通过研究原型病原体,我们可以扩大照亮的区域,获取更多关于病原体家族的知识。而在这个比喻中的黑暗区域,特别是资源匮乏且生物多样性高的地方,可能潜藏着新的病原体,但由于缺乏基础设施和资源,无法进行全面研究。
CEPI首席执行官Richard Hatchett博士表示,“WHO的流行病和大流行病研究准备科学框架是世界在应对措施开发方面的一个重要转变,得到了CEPI的强烈支持。这一框架将帮助引导和协调对整个病原体家族的研究,增强世界对未知变种、新兴病原体、动物传播疾病和所谓病原体X的快速反应能力。”
此次报告的优先排序工作涉及来自50多个国家的200多位科学家,他们评估了28个病毒家族和一个核心细菌群体的科学和证据,共计1652种病原体。通过考虑传播模式、毒力和诊断测试、疫苗和治疗方法的可用性,评估了流行病和大流行病的风险。
WHO和CEPI还呼吁全球协调和合作研究,以准备应对潜在的大流行病。WHO总干事Tedros Adhanom Ghebreyesus博士指出,“历史告诉我们,下一次大流行病只是时间问题。重要的是,增加对不同病原体的了解是一项全球性项目,需所有国家的科学家参与。”目前,WHO正在与全球研究机构合作,为每个病原体家族建立一个协作开放研究联盟(CORC),每个家族由一个WHO合作中心作为研究中心。这些CORC将汇集研究人员、开发人员、资助者、监管者和试验专家等,旨在促进更大的研究合作和公平参与,特别是在已知或高度可能传播病原体的地区。
3. 诺华肾病新药Fabhalta获FDA加速批准,显著减少蛋白尿达44%
本周(8月8日),诺华公司(Novartis)宣布其新药Fabhalta®(活性成分:Iptacopan)获得美国食品药品监督管理局(FDA)的加速批准,用于减少患有原发性IgA肾病(IgAN)且存在快速疾病进展风险成年患者的尿蛋白水平。
IgAN是一种罕见的进展性疾病,每年全球大约有25人每百万人口被诊断为IgAN。由于免疫系统攻击肾脏,导致IgAN患者的肾小球炎症和尿蛋白升高。尽管现有标准治疗方法存在,仍有多达50%的IgAN患者在确诊后10至20年内进展为肾衰竭。这些患者通常需要进行维持透析和/或肾脏移植。
Fabhalta是首个针对IgAN患者的补体抑制剂。补体系统的异常激活被认为是IgAN病理发生的关键因素。Fabhalta通过抑制替代补体途径,有效减少了IgAN者的蛋白尿水平。在APPLAUSE-IgAN研究的中期分析中,Fabhalta相较于安慰剂表现出显著的治疗效果,达到44%的蛋白尿减少,而安慰剂组仅为9%。这一结果在各个亚组中(包括年龄、性别、种族、基线eGFR和蛋白尿水平等)均表现一致,显示了广泛的适用性。
除了Fabhalta,诺华还在开发两种用于IgAN治疗的实验性药物——atrasentan和zigakibart。Atrasentan是一种口服内皮素受体拮抗剂,目前处于FDA审批的申报阶段;而zigakibart是一种抗APRIL单克隆抗体,正在进行三期临床试验。这些药物以不同的作用机制为IgAN患者提供了更多的治疗选择,展示了诺华在肾病治疗领域的持续承诺。
总的来说,Fabhalta的获批标志着诺华在罕见肾病治疗领域的重大进展,为IgAN患者带来了新的希望。通过针对补体替代途径,Fabhalta为临床医生提供了一种有效减少尿蛋白的治疗方法,有望改善患者的长期预后。
参考:
1. Ben Fidler. Lilly obesity drug shows heart benefit in late-stage trial. Published Aug. 1, 2024. Available from: https://www.biopharmadive.com/news/lilly-zepbound-heart-failure-glp-1-study-results/723058/
2. Lilly. Lilly's tirzepatide successful in phase 3 study showing benefit in adults with heart failure with preserved ejection fraction and obesity. August 1, 2024. Available from: https://investor.lilly.com/news-releases/news-release-details/lillys-tirzepatide-successful-phase-3-study-showing-benefit
3. WHO. CEPI and WHO urge broader research strategy for countries to prepare for the next pandemic. 1 August 2024. Available from: https://www.who.int/news/item/01-08-2024-cepi-and-who-urge-broader-research-strategy-for-countries-to-prepare-for-the-next-pandemic
4. Novartis. Novartis receives FDA accelerated approval for Fabhalta® (iptacopan), the first and only complement inhibitor for the reduction of proteinuria in primary IgA nephropathy (IgAN). Aug 08, 2024. Available from:https://www.novartis.com/news/media-releases/novartis-receives-fda-accelerated-approval-fabhalta-iptacopan-first-and-only-complement-inhibitor-reduction-proteinuria-primary-iga-nephropathy-igan
5. Sriparna Roy. US FDA approves Novartis' kidney disease drug. August 8, 2024. Available from:https://www.reuters.com/business/healthcare-pharmaceuticals/us-fda-approves-novartis-kidney-disease-drug-2024-08-07/
原创文章:方舟健客版权所有,未经许可不得转载。