治疗性mRNA疫苗显著抑制HPV相关恶性肿瘤,还能与PD-L1抗体协同延长生存?
 学术前沿官方号
学术前沿官方号人类乳头瘤病毒(HPV)感染与多种人类癌症有关,尤其是高危型HPV16和HPV18,它们是宫颈癌、肛门癌、阴茎癌、外阴癌、阴道癌和头颈癌的主要病因。尽管已有预防性疫苗可降低HPV感染和相关恶性肿瘤的风险,但对于已经感染的个体,现有治疗手段效果有限。因此,开发针对已存在高危HPV感染和病变的治疗性HPV疫苗具有迫切的临床需求。本研究旨在开发一种脂质纳米颗粒(LNP)包裹的mRNA治疗性疫苗mHTV-03E2,同时针对HPV16和HPV18的E2/E6/E7抗原,以期为治疗由HPV16或HPV18感染引起的恶性肿瘤提供新策略。
一、研究方法
研究团队采用了脂质纳米颗粒(LNP)技术,将编码HPV16和HPV18的E2/E6/E7抗原的mRNA封装于LNP中,形成了mHTV-03E2疫苗。通过在C57BL/6小鼠模型中进行疫苗接种,评估了疫苗的免疫原性和抗肿瘤效果。研究中使用了酶联免疫斑点法(ELISpot)和细胞内细胞因子染色(ICS)流式细胞术来检测疫苗诱导的特异性细胞免疫反应。
二、研究结果
1. mHTV-03E2 HPV mRNA-LNP疫苗显示出比其他候选疫苗更优越的免疫原性
在小鼠模型中,该疫苗诱导了针对HPV16和HPV18 E6/E7抗原的强烈的特异性细胞免疫反应,具体表现为IFN-g和IL-2效应细胞因子分泌的显著增加,以及E6/E7特异性CD8+和CD4+ T细胞反应的增强。这些结果通过ELISpot和ICS流式细胞术检测得到验证,与阴性对照组相比具有显著差异(p < 0.001)。mHTV-03E2疫苗的这种高效免疫激活能力,为开发针对高危HPV相关肿瘤的治疗性疫苗提供了有力的实验依据。
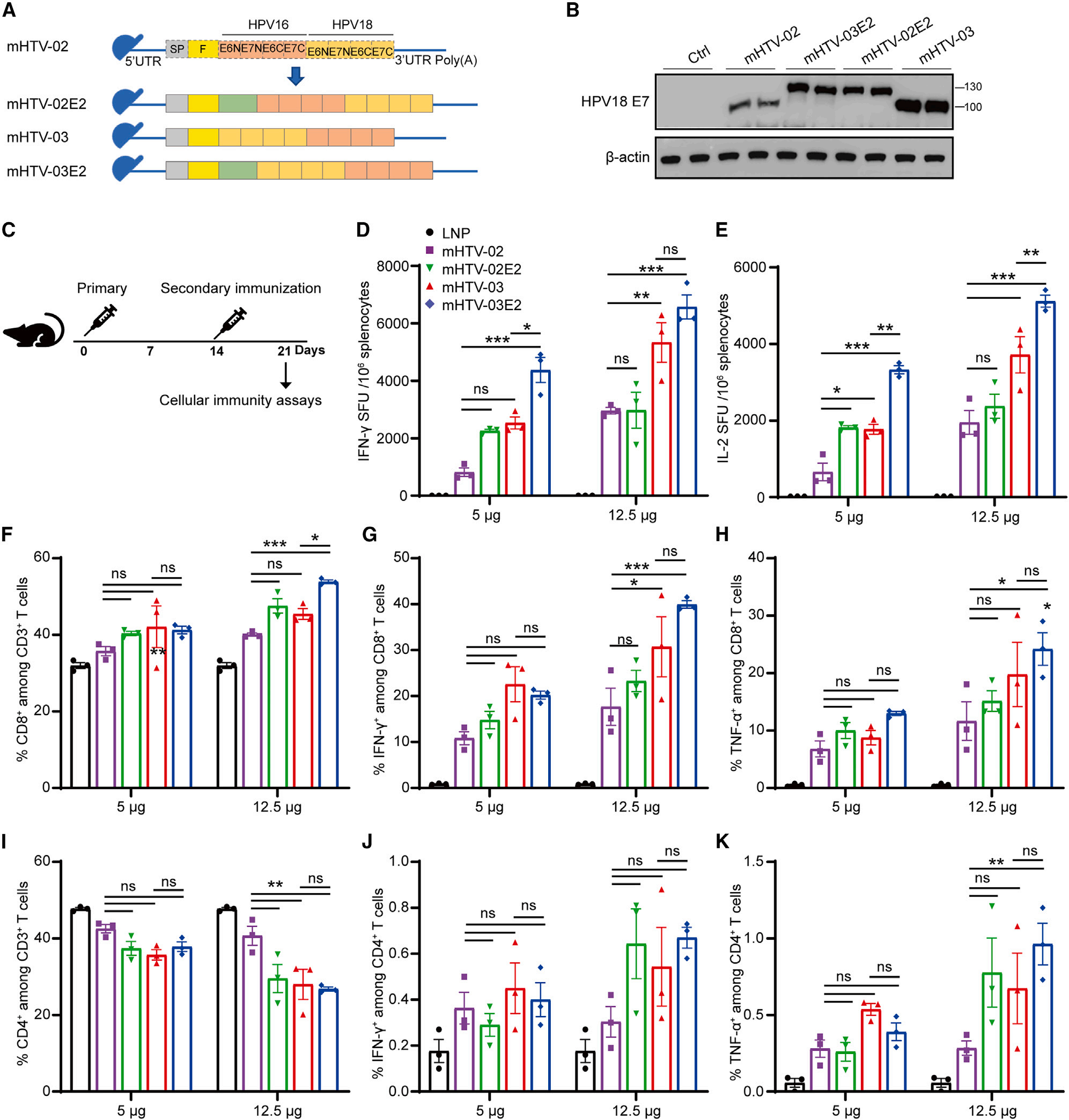
mHTV mRNA-LNP疫苗在体内诱导了针对HPV16/HPV18 E6/E7抗原的显著T细胞免疫反应
2. mRNA疫苗中不同抗原的免疫原性
在mRNA疫苗中,不同抗原的免疫原性研究表明,mHTV-03E2疫苗在三次免疫后显著增强了E6/E7特异性的脾细胞T细胞反应,尤其是针对HPV18 E6和HPV16 E7的反应更为强烈。此外,疫苗接种后,血清中E2特异性IgG抗体滴度显著升高,而抗E6/E7抗体水平相对较低。这些发现表明mHTV-03E2疫苗不仅激活了针对HPV抗原的细胞免疫,还诱导了E2特异性的体液免疫,为HPV16和HPV18驱动的癌症治疗提供了新的策略。
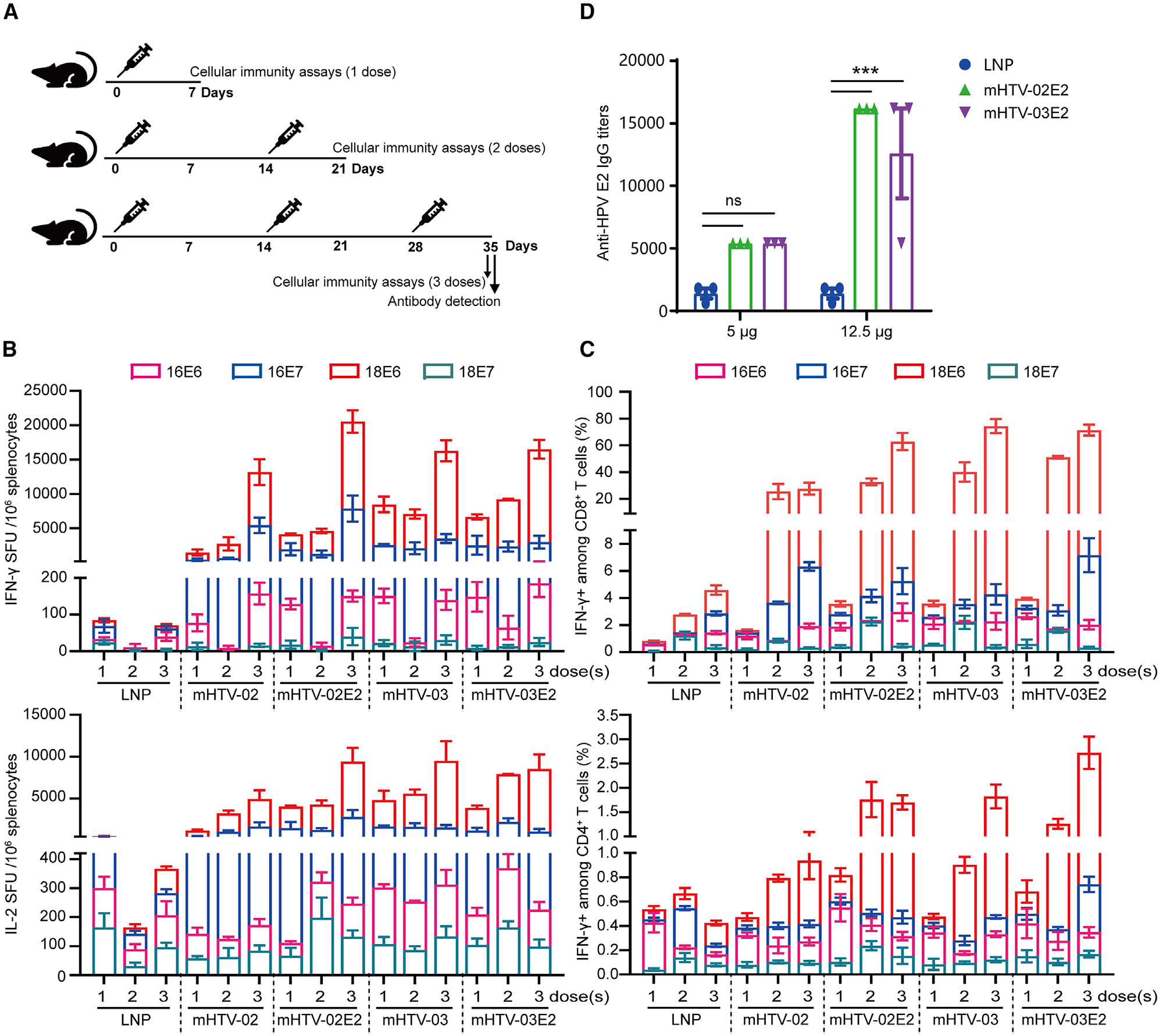
mHTV疫苗的免疫原性
3. HPV mRNA疫苗对TC-1肿瘤模型的治疗效应
在TC-1肿瘤模型中,HPV mRNA疫苗展现了显著的治疗效应。mHTV-03E2疫苗通过肌肉注射显著抑制了肿瘤生长,并显著延长了动物的生存期。值得注意的是,与mHTV-02和mHTV-03相比,包含E2抗原的mHTV-02E2和mHTV-03E2显示出相似的治疗效力,表明E2的融合并未干扰由E6和E7抗原介导的T细胞免疫。此外,mHTV-03E2在首次治疗后15天,以治疗/对照(T/C)比值3.09显著抑制了肿瘤生长(p < 0.001)。长期抗肿瘤功能测试显示,经mHTV治疗后肿瘤完全消退的小鼠在对侧背部皮肤重新接种相同TC-1肿瘤细胞后,所有小鼠均拒绝了肿瘤细胞的再次挑战,并至少在接下来的42天内保持无肿瘤状态,表明了对E6/E7抗原的长期免疫记忆。这些结果支持mHTV-03E2疫苗在治疗HPV16或HPV18感染引起的恶性肿瘤方面的潜力。
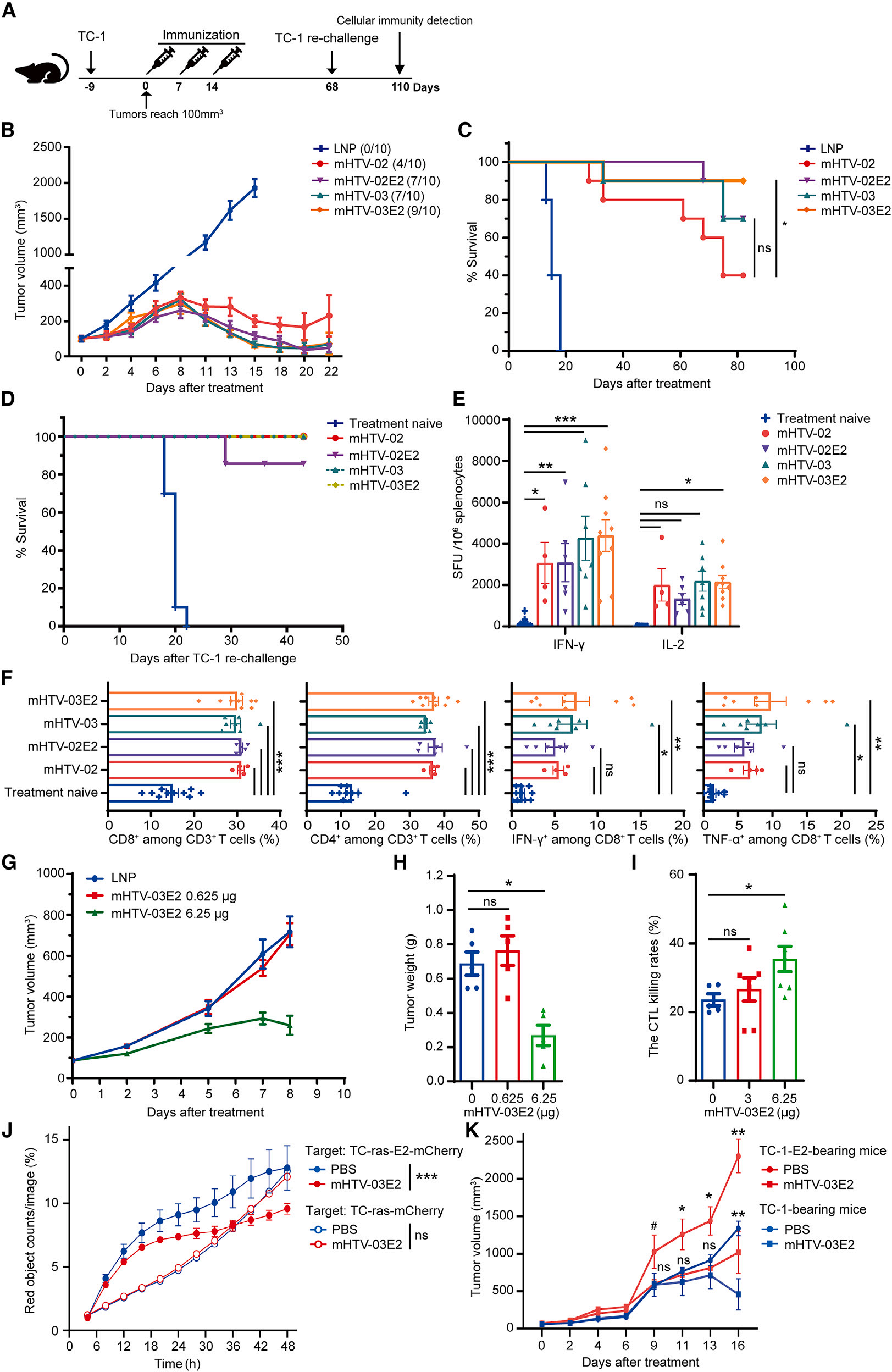
mHTV疫苗在TC-1肿瘤模型上的治疗效果
4. mHTV-03E2疫苗接种在小鼠肿瘤中诱导的免疫细胞浸润
mHTV-03E2疫苗接种在小鼠肿瘤模型中显著促进了免疫细胞的浸润。接种后,肿瘤组织中CD8+和CD4+ T细胞的比例显著增加,特别是通过肌肉注射或肿瘤内注射疫苗后。这些T细胞中,效应记忆T细胞(Tem)的比例显著提高,表明疫苗能够促进记忆T细胞的生成,增强免疫应答的持久性。此外,通过多重免疫组化分析,观察到接种疫苗的小鼠肿瘤中CD8+ T细胞的增殖率显著提高,其中57%至44%的细胞通过Ki-67染色显示高度增殖。这些发现表明,mHTV-03E2疫苗通过增强肿瘤特异性T细胞的浸润和增殖,有效促进了抗肿瘤免疫反应。
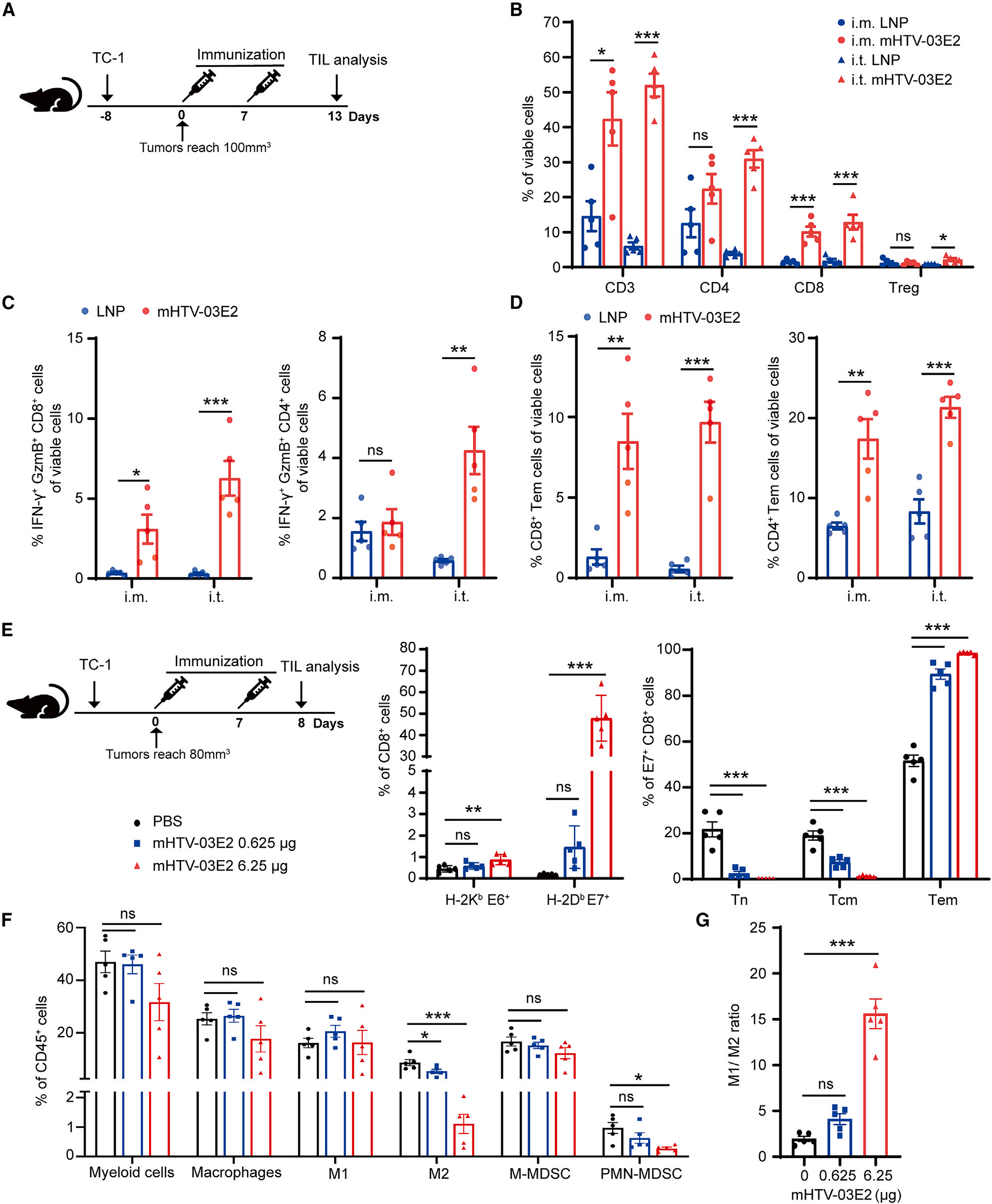
mHTV疫苗接种在小鼠肿瘤中诱导的免疫细胞浸润
5. HPV疫苗治疗后小鼠肿瘤中的免疫细胞特征
在HPV疫苗治疗后的小鼠肿瘤中,免疫细胞的特征化分析揭示了mHTV-03E2疫苗对肿瘤微环境的显著影响。接种疫苗的小鼠肿瘤组织中CD8+ T细胞的频率显著增加,其中57%和44%的细胞通过Ki-67染色显示高度增殖(p < 0.001)。此外,CD4+ T细胞的频率和增殖也受到影响。mHTV-03E2疫苗还显著提高了肿瘤中CD11c+树突细胞的数量,这可能有助于提高抗原呈递效率。同时,肿瘤细胞凋亡标记物Cleaved Caspase 3(CC3+)的水平显著增加,表明疫苗诱导了肿瘤细胞的凋亡。这些发现强调了mHTV-03E2疫苗在激活肿瘤特异性T细胞反应、促进树突细胞介导的抗原呈递以及诱导肿瘤细胞凋亡方面的潜力。
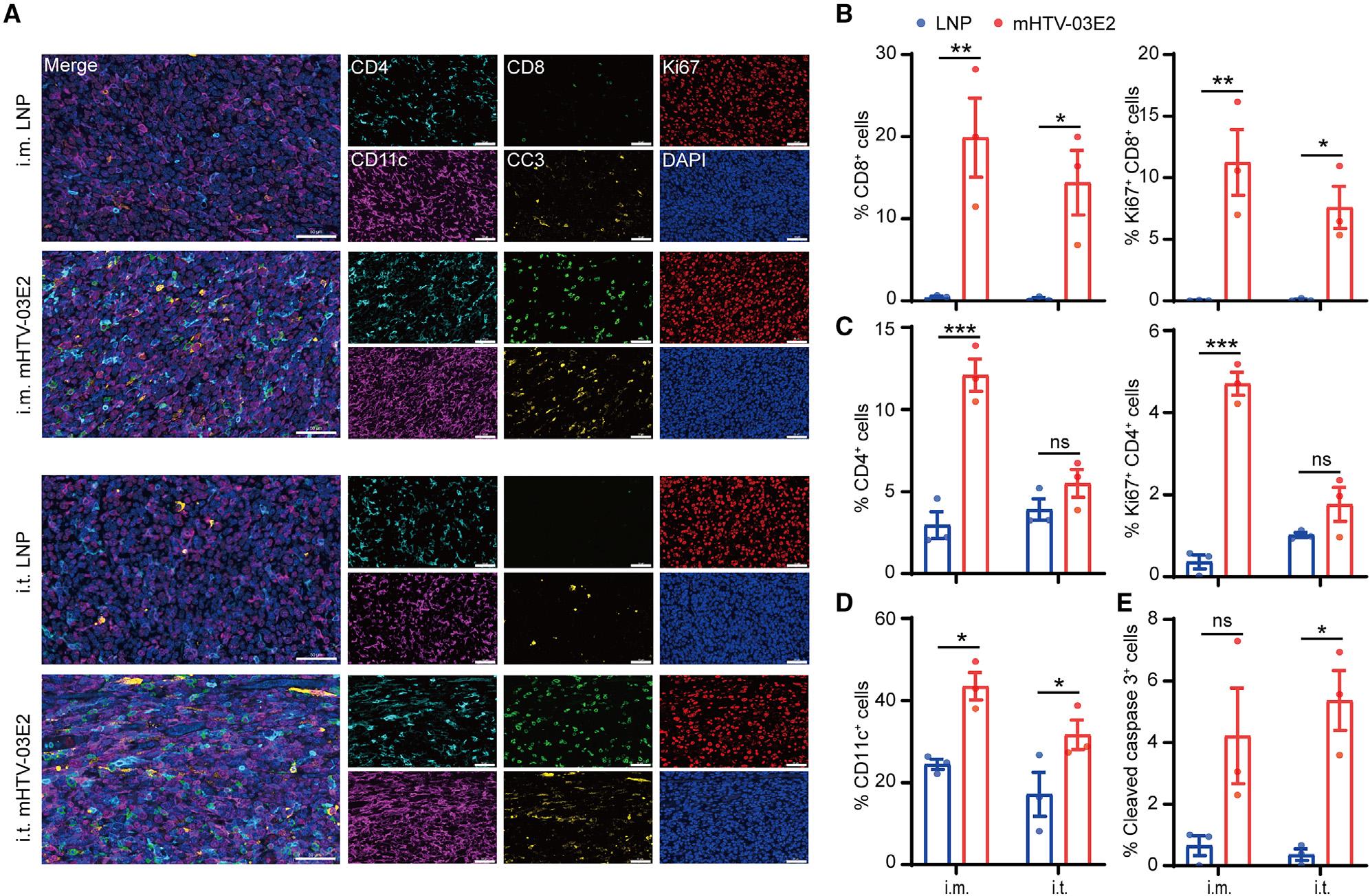
肿瘤组织中免疫细胞的分布和浸润特征
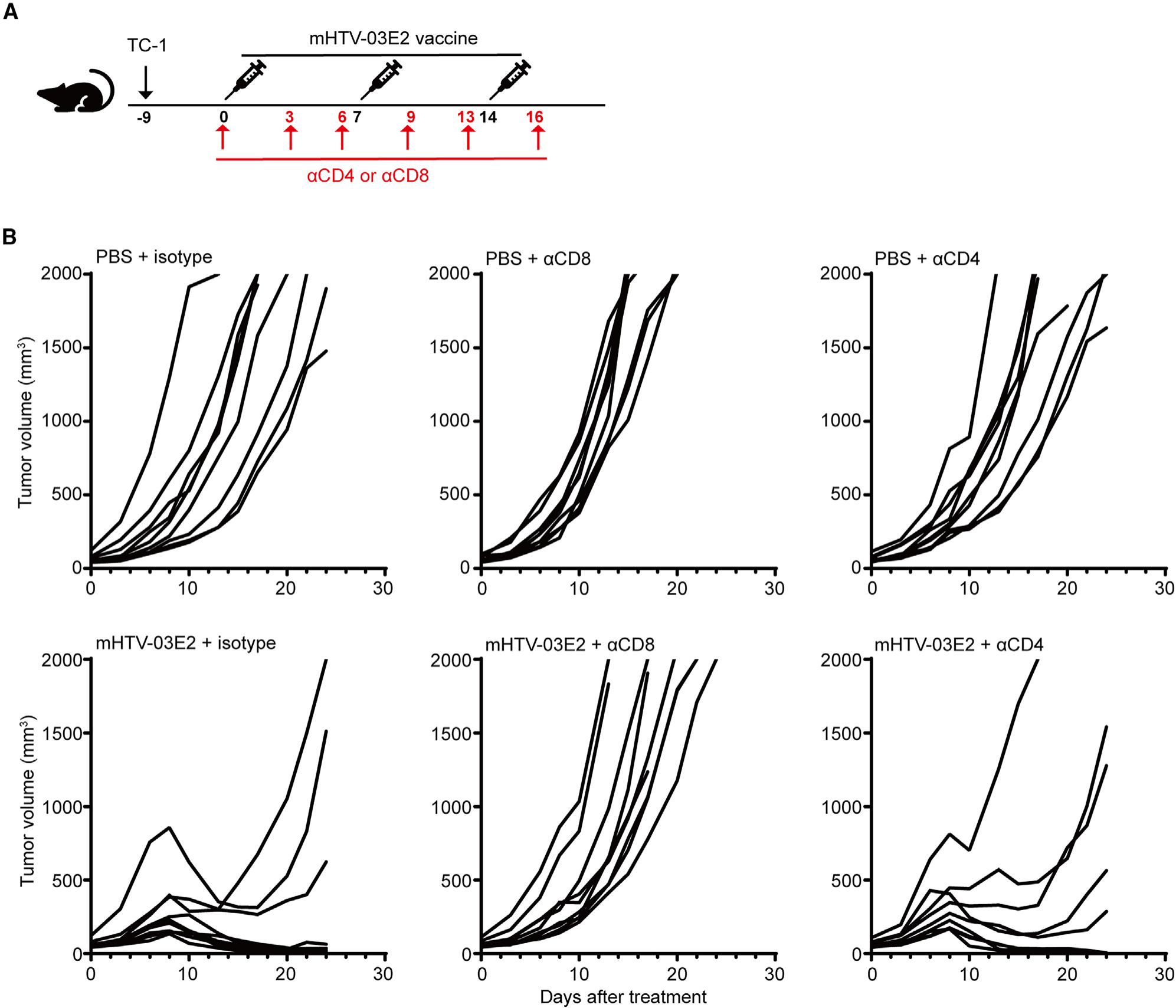
CD8+ T细胞是mHTV-03E2诱导的TC-1肿瘤模型中抗肿瘤免疫所需的
6. mHTV-03E2疫苗与免疫检查点阻断协同抑制肿瘤
mHTV-03E2疫苗与免疫检查点阻断剂联合使用,在肿瘤抑制方面表现出协同效应。在TC-1肿瘤模型中,mHTV-03E2疫苗与抗PD-L1抗体(aPD-L1)的联合治疗显著延迟了肿瘤生长并延长了动物生存期,与单独使用aPD-L1相比,显示出明显的剂量依赖性协同效应(p < 0.001)。这一发现为HPV相关肿瘤的治疗提供了新的策略。
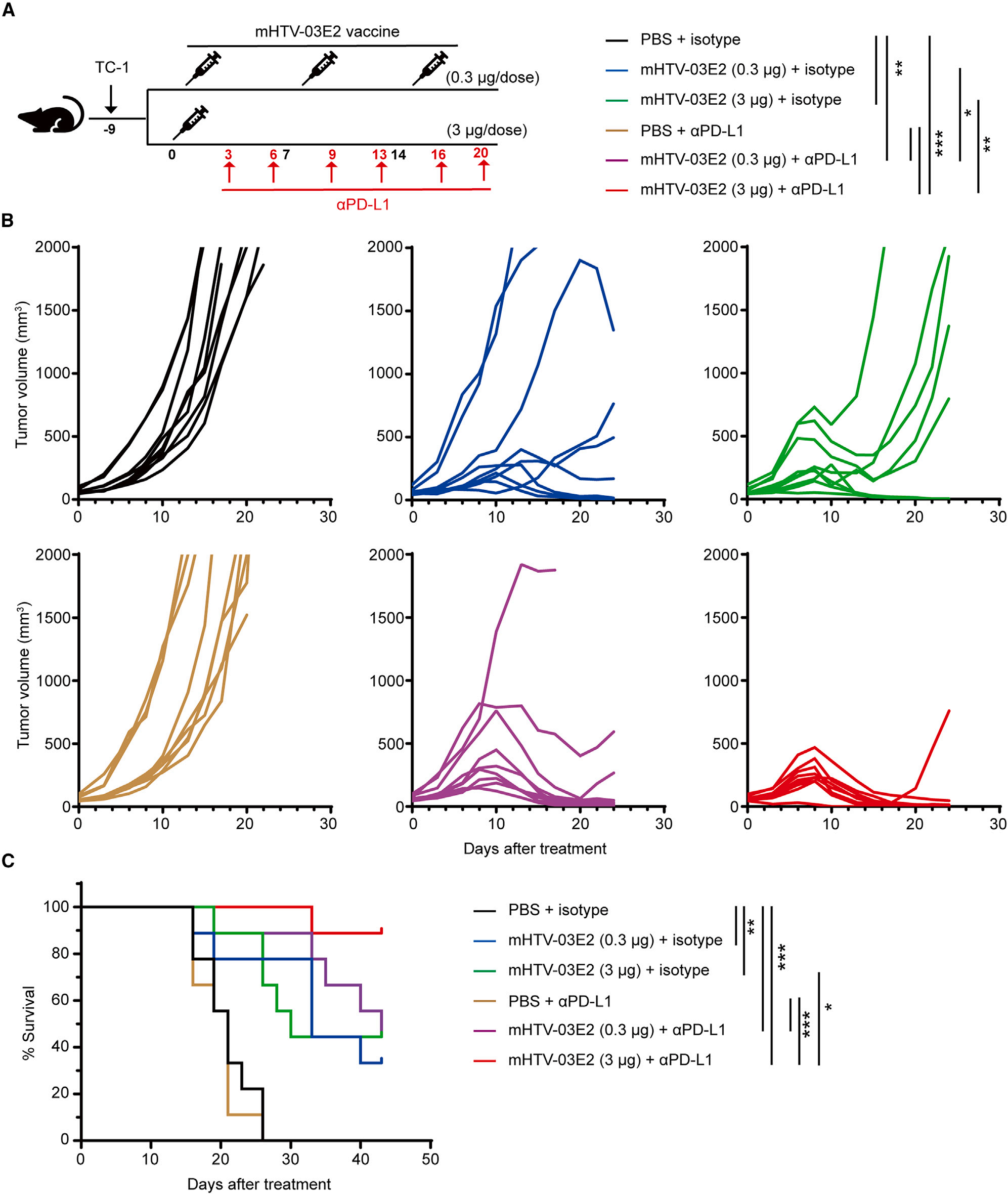
mHTV-03E2疫苗联合PD-L1抗体抑制肿瘤生长
三、讨论
本研究深入分析了mHTV-03E2 mRNA治疗性疫苗针对HPV16和HPV18 E2/E6/E7抗原的免疫反应。疫苗成功诱导了强烈的细胞免疫反应,特别是显著增加了肿瘤组织中增殖性CD4+和CD8+ T细胞以及多功能CD8+ T细胞的数量,这些细胞是T细胞免疫治疗效应的关键。此外,耗竭实验进一步证实了CD8+ T细胞在肿瘤抑制中的至关重要作用。
研究还强调了mHTV-03E2疫苗与PD-L1抗体联合使用时的协同效应,其显著抑制了肿瘤生长并延长了动物的生存期。这种协同作用可能有助于将PD-1/PD-L1阻断疗法的应用范围扩展到目前对单药免疫检查点阻断疗法抵抗的患者群体。
此外,mHTV-03E2疫苗诱导的免疫记忆反应在接种后至少4个月内仍然显著,为疫苗提供了长期保护肿瘤复发的潜力。这为mHTV-03E2作为治疗性疫苗用于治疗由HPV16或HPV18感染引起的恶性肿瘤提供了有力的支持。
最后,mHTV-03E2疫苗设计中的关键创新点,包括E2抗原的包含以及E6和E7抗原的重新排列,这可能促进了更有效的抗原处理或识别,从而增强了疫苗的免疫原性。这些发现为未来的临床试验和疫苗的进一步开发提供了科学依据。
结论
mHTV-03E2作为一种新型mRNA治疗性疫苗,在小鼠模型中显示出了良好的抗肿瘤效果和免疫原性,为高危HPV相关恶性肿瘤的治疗提供了新的可能性。然而,从实验室研究到临床应用,mHTV-03E2疫苗仍需跨越多道障碍,包括确保其在人类中的安全性、有效性以及长期免疫保护效果。此外,疫苗的成本效益、生产可及性和分发策略也是决定其能否广泛应用于临床实践的关键因素。
参考文献
【1】Wang J, Wang Q, Ma L, et al. Development of an mRNA-based therapeutic vaccine mHTV-03E2 for high-risk HPV-related malignancies. Mol Ther. Published online May 6, 2024. doi:10.1016/j.ymthe.2024.04.036.
原创文章:方舟健客版权所有,未经许可不得转载。