房颤背后的基因风暴:JAMA子刊揭示TET2和ASXL1突变的秘密
 学术前沿官方号
学术前沿官方号研究表明,随着年龄的增长,造血干细胞中的获得性基因突变逐渐积累,某些突变克隆因具备生存优势得以扩增并进入外周血,这一过程被称为不确定潜能克隆造血(CHIP)。过去的研究主要将CHIP与血液恶性肿瘤风险联系在一起,如CHIP可以通过改变DNA损伤应答、改变转录程序、改变表观遗传学等增加恶性疾病的患病风险,显著升高携带者血液系统恶性肿瘤的发病率。但近年来,越来越多的证据表明CHIP可能在心血管疾病中扮演重要角色。然而,CHIP与房颤的关联性尚未被系统研究。
在《美国医学会杂志》(JAMA) 子刊最新发表的研究中,一项开创性研究揭示了CHIP与房颤之间的惊人关联。尽管人类衰老常伴随慢性炎症状态,称为“炎症性衰老”,然而这种状态如何与房颤的高发病率联系起来,至今未有定论。此次研究利用动脉粥样硬化风险社区(Atherosclerosis Risk in Communities, ARIC)研究和英国生物银行(UK Biobank, UKB)两个大型群体队列数据,首次探讨了CHIP中特定基因突变(如TET2和ASXL1)与房颤、炎症和心脏结构变化之间的复杂关系。这项研究为我们提供了一个全新的视角,帮助理解克隆性造血如何通过炎症和心脏重塑途径,增加房颤的风险。
一、 研究方法
研究分析了来自ARIC和UKB两大队列的成人数据,探讨CHIP与房颤之间的关联。ARIC队列于1987-1989年间在美国四个社区招募,UKB队列于2006-2010年在英国招募。研究排除了在基线时有性别不一致、血液恶性肿瘤、二尖瓣狭窄或二尖瓣手术史的参与者。在UKB中,还排除了患有肥厚型心肌病和先天性心脏病的参与者。CHIP的识别基于外周血DNA的外显子测序数据,使用GATK MuTect2突变检测工具,聚焦于促进造血干细胞克隆扩增的特定基因变异,变异等位基因频率(VAF)≥2%被定义为CHIP,≥10%则定义为大CHIP。
主要结局事件为新发的房颤,ARIC通过心电图、医院出院诊断和死亡证明确认,UKB通过访谈和住院ICD-9/ICD-10代码确认。使用多变量Cox比例风险模型调整了多种混杂因素,包括年龄、性别、种族、中心、高血压、估算肾小球滤过率、糖尿病、吸烟状态、饮酒、体重指数、冠心病和心力衰竭。通过逆方差加权法进行汇总风险比(HR)分析。
二、 研究结果
1. 基线特征和CHIP频率
研究纳入了199,982名成人参与者,来自ARIC(4,131名,占2.1%)和UKB(195,851名,占97.9%)队列。在ARIC队列中,4131名参与者中1019名(24.7%)存在任何类型的CHIP,478名(11.6%)具有大CHIP。DNMT3A、TET2和ASXL1变异的携带者分别占11.8%、5.6%和2.2%。这些基因变异与房颤风险增加有关,特别是大型TET2和ASXL1 CHIP,可能为心血管疾病的风险分层和个体化治疗提供新的生物标志物。
2. 房颤的累积发病率
排除了2,767名基线时已有房颤的参与者后,在剩余的197,209名参与者中,ARIC队列中位随访时间为7.0年(IQR=5.3-7.7),UKB队列中位随访时间为12.2年(IQR=11.3-13.0),分别发生了417和8,938例新发房颤事件。每1000人/年房颤事件发生率在无CHIP、CHIP和大CHIP的参与者中分别为:ARIC队列为15.1(95% CI: 13.3-16.9)、18.4(95% CI: 14.8-22.0)和20.8(95% CI: 15.1-26.5);UKB队列为3.8(95% CI: 3.7-3.9)、5.3(95% CI: 4.9-5.7)和5.8(95% CI: 5.2-6.4)。在DNMT3A、TET2和ASXL1携带者中,ARIC队列的房颤发生率分别为15.1(95% CI: 10.4-19.7)、24.8(95% CI: 15.9-33.7)和34.0(95% CI: 15.5-52.5);UKB队列为5.0(95% CI: 4.5-5.4)、6.3(95% CI: 5.3-7.3)和9.3(95% CI: 7.0-11.6)。
3. CHIP与房颤的关联
在综合分析的全调整模型中,与无CHIP相比,大CHIP的存在与房颤相关(HR=1.12,95% CI, 1.01-1.25,P=0.04),而任何CHIP的存在与房颤则无显著关联(HR=1.02,95% CI, 0.94-1.11,P=0.57)。基因特异性分析显示,DNMT3A与房颤无关联;然而,任何TET2 CHIP(HR=1.18,95% CI, 1.01-1.38,P=0.04)、大TET2 CHIP(HR=1.29,95% CI, 1.05-1.59,P=0.02)、任何ASXL1 CHIP(HR=1.33,95% CI, 1.02-1.73,P=0.03)和大ASXL1 CHIP(HR=1.45,95% CI, 1.02-2.07,P=0.04)与房颤风险增加有关。
4. CHIP与炎症标志物
在ARIC队列中,CHIP携带者和无CHIP参与者的高敏C-反应蛋白(hs-CRP)和白细胞介素-18(IL-18)水平相似。白细胞介素-6(IL-6)水平在无CHIP与大DNMT3A或ASXL1 CHIP参与者间相似,但在大TET2 CHIP参与者中显著增加(中位数4.19 pg/mL vs 2.91 pg/mL,P=0.004)。仅IL-6水平与房颤独立相关(HR=1.26,95% CI: 1.13-1.41,P=6.3 × 10⁻⁵)。
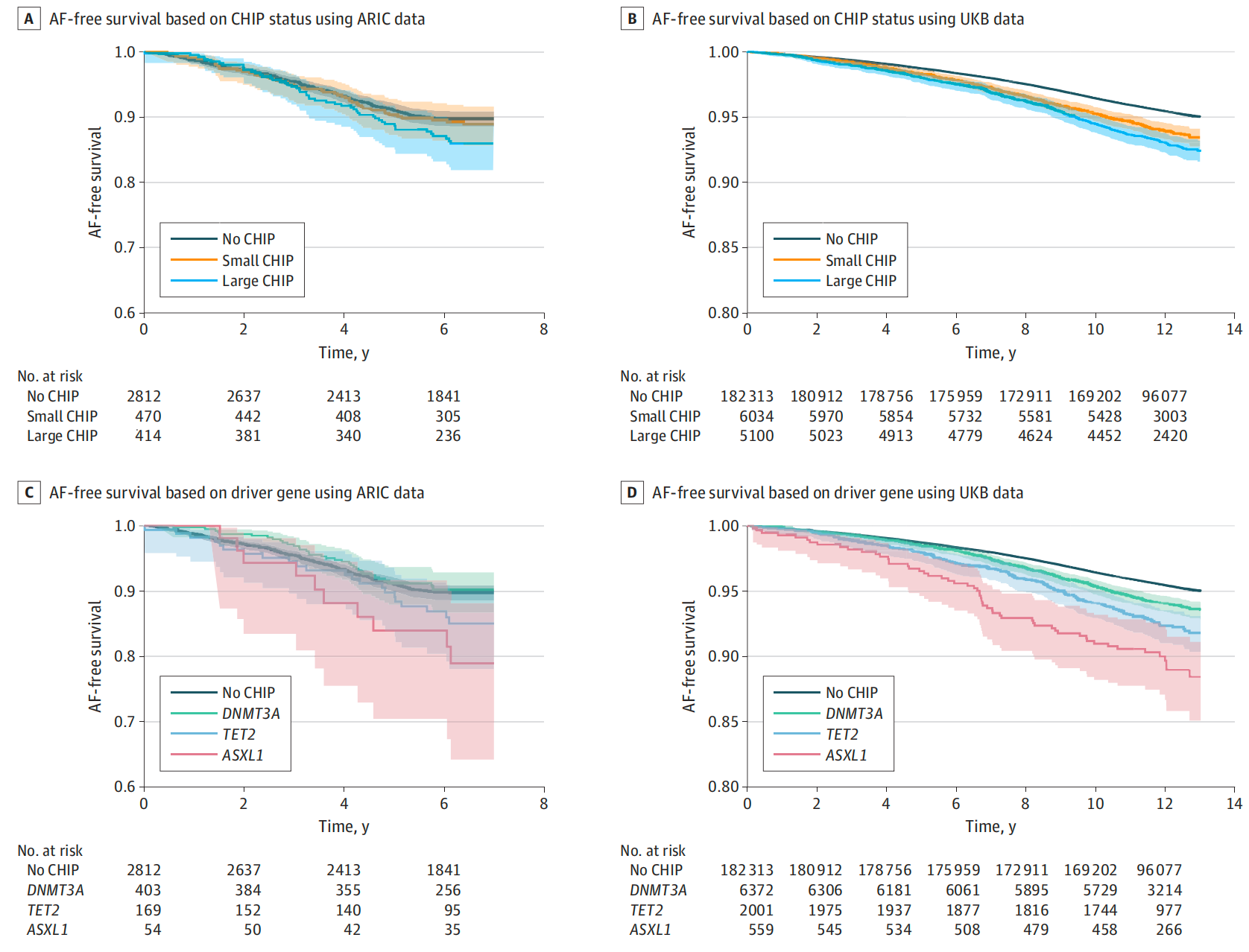
基于CHIP状态和驱动基因变异的房颤的无事件存活Kaplan-Meier曲线
图A和B,根据CHIP状态显示了无CHIP的个体、具有小CHIP的个体和具有大CHIP的个体的AF无事件存活情况。
图C和D,根据驱动基因显示了无CHIP的个体、具有DNMT3A基因变异的个体、具有TET2基因变异的个体和具有ASXL1基因变异的个体的AF无事件存活情况。
5. CHIP与心脏生物标志物
在ARIC队列中,无CHIP与大CHIP(由DNMT3A、TET2或ASXL1驱动)参与者的高敏肌钙蛋白I (hs-TnI)和N末端B型利钠肽前体(NT-proBNP)水平相似,但大ASXL1 CHIP参与者的高敏肌钙蛋白T(hs-TnT)水平显著增加(中位数14.00 ng/L vs 10.00 ng/L,P<0.001)。
6. CHIP与心脏超声检查的心脏重塑
在没有CHIP和具有大片段DNMT3A、TET2或ASXL1 CHIP的参与者之间,左心室射血分数(LVEF)、左心室舒张末期容积指数(EDVi)、左心室收缩末期容积指数(ESVi)和左心房直径指数(LADi)相似。没有CHIP和具有大片段ASXL1 CHIP的参与者之间,左心室质量指数(LVMi)相似。没有CHIP的参与者和具有大片段ASXL1 CHIP的参与者的LVMi中位数(IQR)分别为75.87(65.38-89.15)g/m2和87.39(72.50-112.94)g/m2。
7. TET2/ASXL1状态和生物标志物水平对房颤发生率的影响
在没有CHIP的参与者中,IL-6是唯一与新发房颤相关的炎症标志物。没有CHIP的参与者中,IL-6水平低和IL-6水平高的新发房颤的每1000人/年发生率分别为11.18(95%CI: 9.00-13.36)和17.93(95%CI: 14.97-20.89)。所有心脏生物标志物都与房颤的发生率相关。例如,没有CHIP的参与者中,hs-TnI水平低和hs-TnI水平高的新发房颤的每1000人年发生率分别为9.41(95% CI:7.41-11.41)和16.28(95% CI:7.07-25.49);具有大片段TET2/ASXL1 CHIP的参与者中分别为23.01(95%CI:19.66-26.36)和34.90(95%CI:21.48-48.31)。在心脏超声检查中,与预期一样,LVMi和LADi较大的个体具有较高的房颤发生率;然而,在具有大片段TET2/ASXL1 CHIP的参与者中,LVEF较高的个体具有较高的房颤发生率。
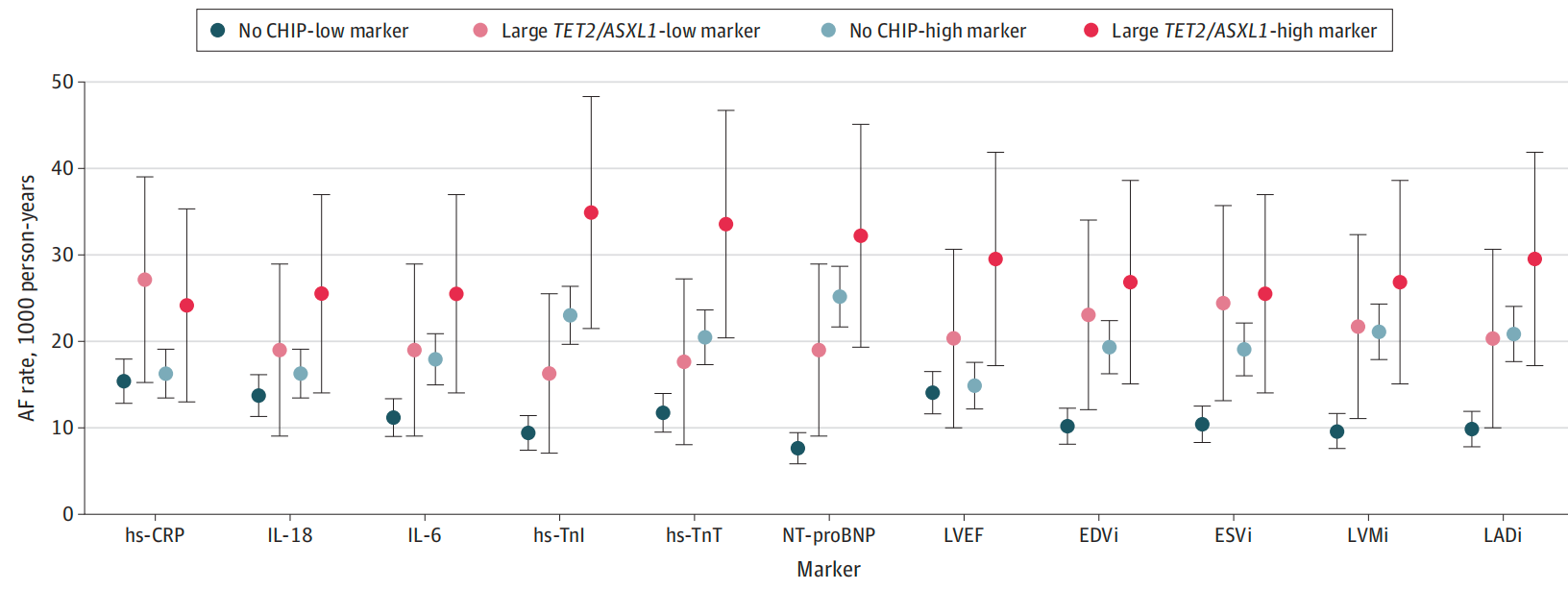
基于TET2/ASXL1状态、炎症标志物水平、心脏生物标志物水平以及超声心动图测量的新发房颤发生率
EDVi,左心室舒张末期容积指数;ESVi,左心室收缩末期容积指数;hs-CRP,高敏C-反应蛋白;hs-TnI,高敏肌钙蛋白I;hs-TnT,高敏肌钙蛋白T;IL-6,白细胞介素-6;IL-18,白细胞介素-18;LADi,左心房直径指数;LVEF,左心室射血分数;LVMi,左心室质量指数;NT-proBNP,N末端前B型钠尿肽。
三、讨论
这项研究揭示了大规模队列研究中常见的CHIP与房颤发生的独立关联,特别是TET2和ASXL1基因变异,而非DNMT3A。TET2基因变异与IL-6水平升高相关,而IL-6是房颤发生的独立预测因子。此外,大片段ASXL1 CHIP与hs-TnT水平升高和LVMi增加有关,这些都是心脏重塑的标志,与房颤风险增加有关。研究结果表明,CHIP可能通过炎症途径和心脏结构变化影响房颤的发生。这些发现在临床上具有重要意义,因为它们提示了CHIP在心血管疾病发展中的潜在作用。
研究还发现IL-6是与CHIP相关的炎症标志物中的一个关键因素,而IL-18和hs-CRP水平与CHIP之间没有明显关联。这表明,IL-6可能在介导CHIP与心血管疾病之间的关联中起到更重要的作用。这些结果强调了炎症在心血管疾病中的关键作用,尤其是在CHIP相关的机制中。
此外,研究指出尽管2%和10%的VAF阈值是任意的,但使用VAF作为CHIP负担的连续度量,其总体发现与分类分析一致。敏感性分析表明,房颤的发展可能独立于冠状动脉心脏病(CHD)和心力衰竭(HF)在TET2突变中观察到,但ASXL1则不然。这可能需要更大的样本量和不同的成像方式来进一步研究。
尽管研究结果有启发性,但也存在一些限制。两个队列之间存在人口学和临床差异,而且染色体测序的方法也有所不同。此外,虽然研究已经进行了全面的调整,但仍存在其他未能控制的潜在混杂因素,例如遗传因素和生活方式因素。此外,部分参与者的生物标志物数据有限,使得中介分析的可能性受到了限制。
结论
本研究提供了关于CHIP,特别是TET2和ASXL1基因变异与房颤风险之间关联的重要证据。这些发现为理解CHIP在心血管疾病发展中的作用提供了重要线索,并可能为未来的临床管理提供新的治疗靶点。然而,仍需要进一步的研究来验证这些发现,并探索潜在的干预措施以降低患者的心血管风险。未来的研究应考虑更广泛的遗传多样性,并进一步验证这些关联在不同人群中的一致性。
参考文献
【1】Saadatagah S, Naderian M, Uddin M, et al. Atrial Fibrillation and Clonal Hematopoiesis in TET2 and ASXL1. JAMA Cardiol. 2024;9(6):497-506. doi:10.1001/jamacardio.2024.0459.
原创文章:方舟健客版权所有,未经许可不得转载。