Nature Medicine: PD-L1单抗+抗血管生成+化疗带来ES-SCLC一线治疗新选择
 学术前沿官方号
学术前沿官方号太长不看版
贝莫苏拜单抗(PD-L1抑制剂)联合安罗替尼(多靶点抗血管生成药物)与化疗(依托泊苷/卡铂)用于广泛期小细胞肺癌(ES-SCLC)一线治疗,相比化疗显著延长OS和PFS(中位OS19.3 个月vs. 11.9个月;中位PFS6.9 个月vs.4.2 个月)。
小细胞肺癌(SCLC)是一种侵袭性极强的肺癌类型,约占所有肺癌病例的15%。广泛期(ES-SCLC)患者预后尤其不佳,五年生存率仅1%-5%。近年来免疫检查点抑制剂(ICIs)的应用为SCLC的治疗带来了新的希望,而抗血管生成治疗已被证明在多瘤种中可以增强ICIs的疗效。
贝莫苏拜单抗是一种人源化抗PD-L1抗体,显示出与其他ICIs相似的抗肿瘤活性。安罗替尼作为一种多靶点抗血管生成药物,已在中国获批用于ES-SCLC的三线治疗。本研究旨在探索贝莫苏拜单抗联合安罗替尼和化疗在ES-SCLC中的疗效和安全性。
研究设计
本研究为一项在中国72个中心进行的双盲、随机、安慰剂对照的III期临床试验。研究对象为18至75岁、组织学确诊的ES-SCLC患者,且未接受过针对ES-SCLC的系统治疗。排除标准包括既往接受过抗血管生成药物或其他PD-L1抑制剂治疗,有症状或未经治疗的脑转移,以及需要系统治疗的自身免疫性疾病。
研究共纳入738名患者,随机分配至三个治疗组:贝莫苏拜单抗+安罗替尼+依托泊苷/卡铂(EC)组(n=246)、安罗替尼+EC组(n=245)、单独EC组(n=247)。所有治疗均以21天为一个周期。在诱导,患者接受规定的治疗方案,共四个周期。达到完全缓解、部分缓解或稳定疾病的患者将根据之前的随机分配接受维持治疗。治疗持续直至疾病进展、临床效益丧失或不可接受的毒性发生。
研究的主要终点为独立评审委员会(IRC)根据RECIST 1.1评估的无进展生存期(PFS)和总生存期(OS)。次要终点包括研究者评估的PFS、IRC评估的客观反应率(ORR)、疾病控制率(DCR)、反应持续时间(DoR)、6个月和12个月的PFS率、12个月和18个月的OS率、健康相关生活质量(HRQoL)以及安全性。
联合治疗组在多个疗效指标上均表现出显著优势
总生存期(OS)
莫苏拜单抗+安罗替尼+EC组(四药治疗组)的中位OS为19.3个月,显著高于EC组的11.9个月(HR0.61;95%CI:0.47–0.79;P=0.0002)。亚组分析显示,OS改善在多个预设亚组中均一致,包括不同性别、年龄、疾病阶段等。
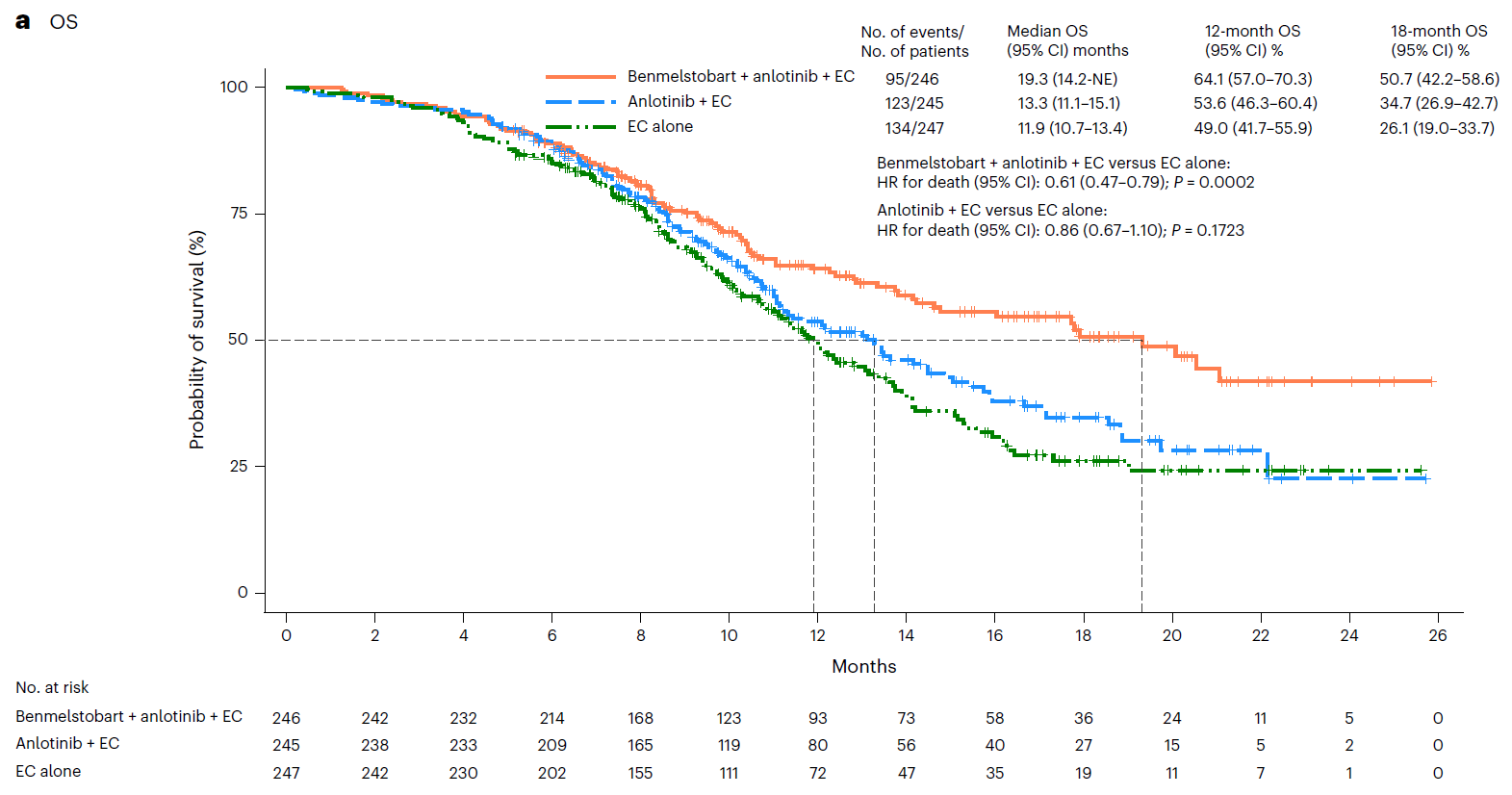 三个治疗组的OS情况(KM曲线)
三个治疗组的OS情况(KM曲线)
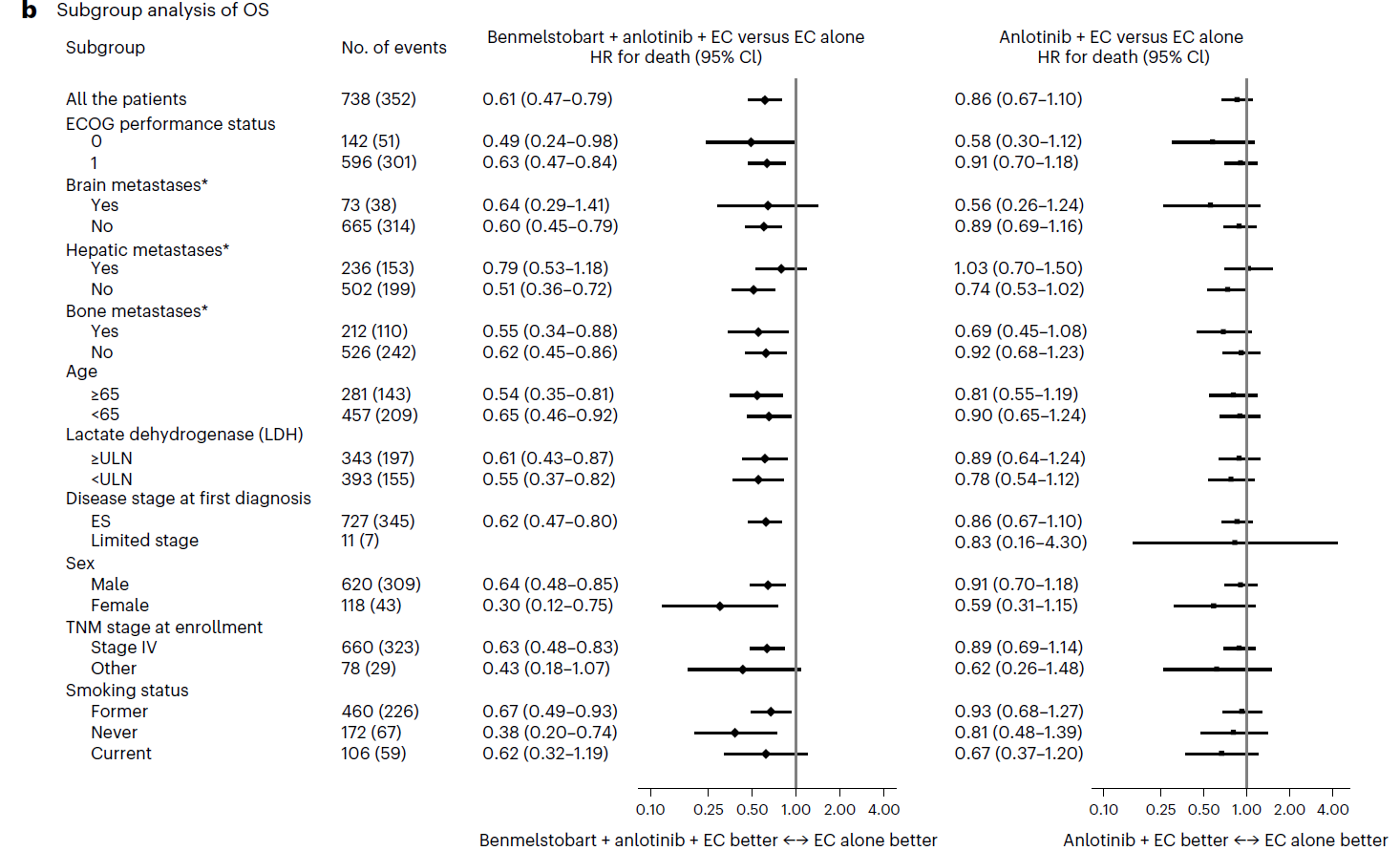 OS亚组分析
OS亚组分析
无进展生存期(PFS)
四药治疗组的中位PFS为6.9个月,显著高于EC组的4.2个月(HR0.32;95%CI:0.26–0.41;P < 0.0001)。安罗替尼+EC组(三药治疗组)的中位PFS为5.6个月,也显著高于EC组(HR0.44;95%CI:0.36–0.55;P < 0.0001)。两组相比EC组的PFS获益可在所有亚组中观察到。
 三个治疗组的PFS情况(KM曲线)
三个治疗组的PFS情况(KM曲线)
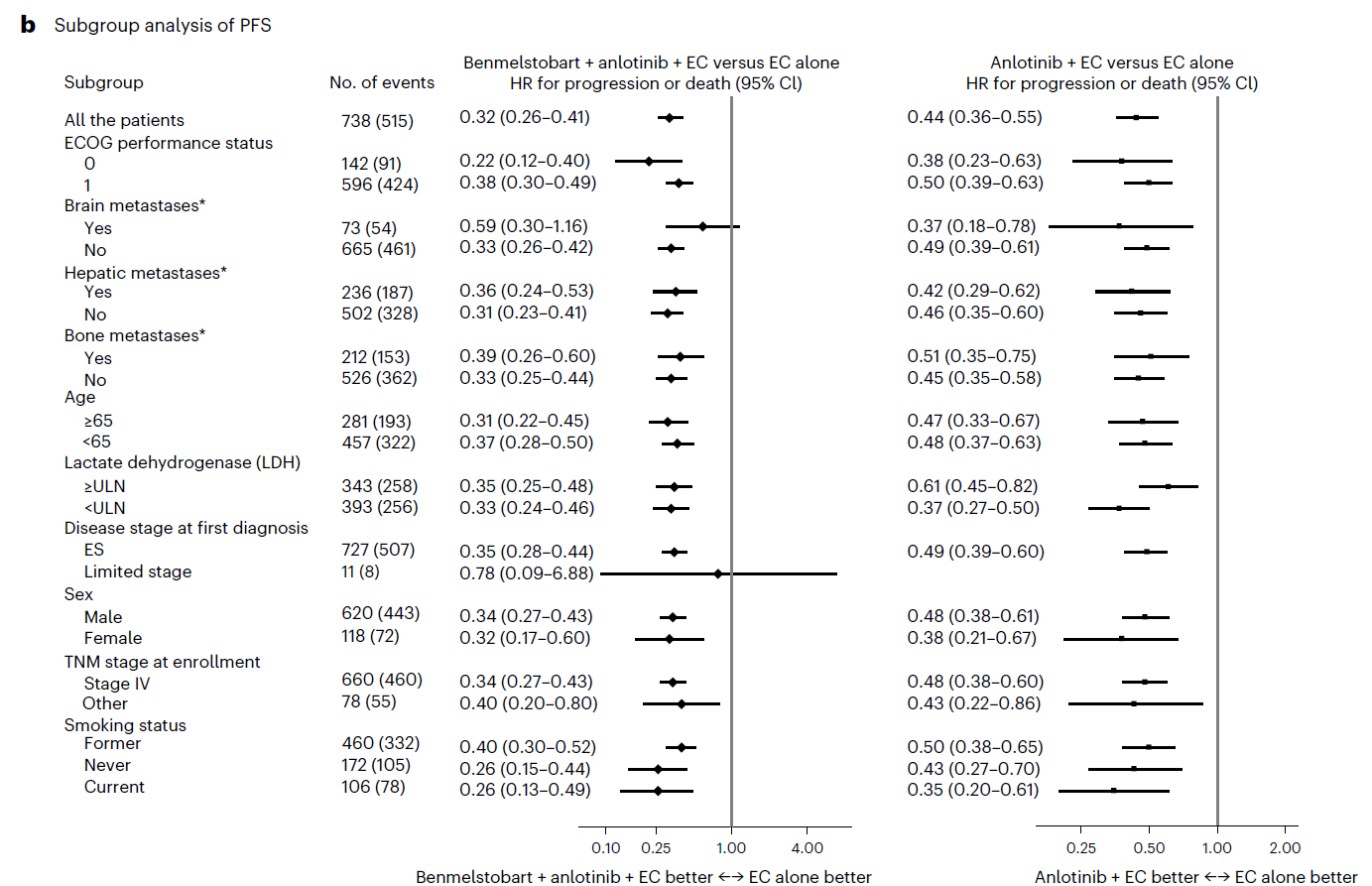 PFS亚组分析
PFS亚组分析
客观反应率(ORR)
四药治疗组、三药治疗组和EC组的ORR分别为81.3%(95%CI:75.9%–86.0%)、81.2%(95%CI:75.8%–85.9%)和66.8%(95%CI:60.6%–72.6%,P=0.0001和P=0.0003)。
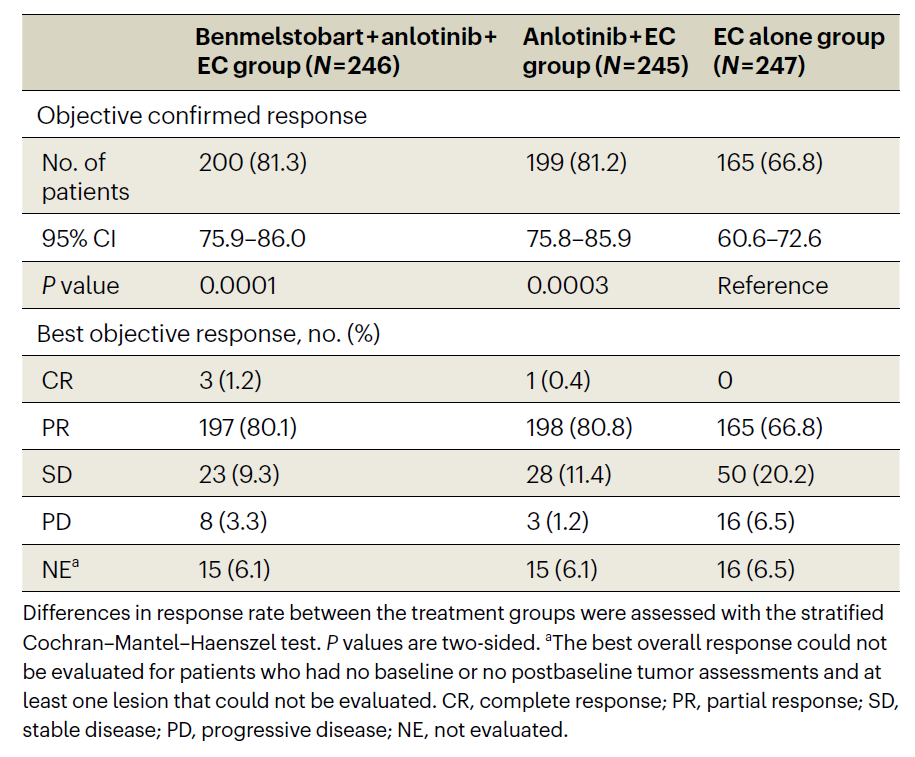 使用RECIST 1.1标准评估的肿瘤反应情况
使用RECIST 1.1标准评估的肿瘤反应情况
疾病控制率(DCR)
四药治疗组的DCR为90.7%,而EC组为87.0%,未达到统计学显著性(P=0.2003);三药治疗组相比EC组DCR有显著改善(92.7% vs 87.0%;P=0.0378)。
反应持续时间(DoR)
四药治疗组、三药治疗组和EC组的中位DoR分别为5.8个月(95%CI:5.5–7.2)、5.5个月(95%CI:4.3–5.6)和3.1(95%CI:2.9–4.1)个月。
安全性
四药及三药治疗组的3级或更高级别的治疗相关不良事件(TRAEs)发生率略高于EC组(93.1% vs 94.3% vs 87%),但这些不良事件大多通过支持性治疗或剂量调整得到了有效管理。
健康相关生活质量(HRQoL)
所有治疗组在治疗期间均显示出从基线开始的整体改善趋势,但各组间在欧洲生活质量视觉模拟量表(EQ-VAS)评分上未发现显著差异。
讨论
本研究显示贝莫苏拜单抗(抗PD-L1单抗)联合安罗替尼(多靶点抗血管生成药)和化疗作为ES-SCLC一线治疗,能够显著改善患者的预后,有潜力成为ES-SCLC一线治疗的新选择。特别是OS的显著延长和广泛的亚组一致性,为临床治疗提供了重要参考。
参考文献
Cheng Y, Chen J, Zhang W, et al. Benmelstobart, anlotinib and chemotherapy in extensive-stage small-cell lung cancer: a randomized phase 3 trial. Nat Med. Published online July 11, 2024. doi:10.1038/s41591-024-03132-1.
原创文章:方舟健客版权所有,未经许可不得转载。