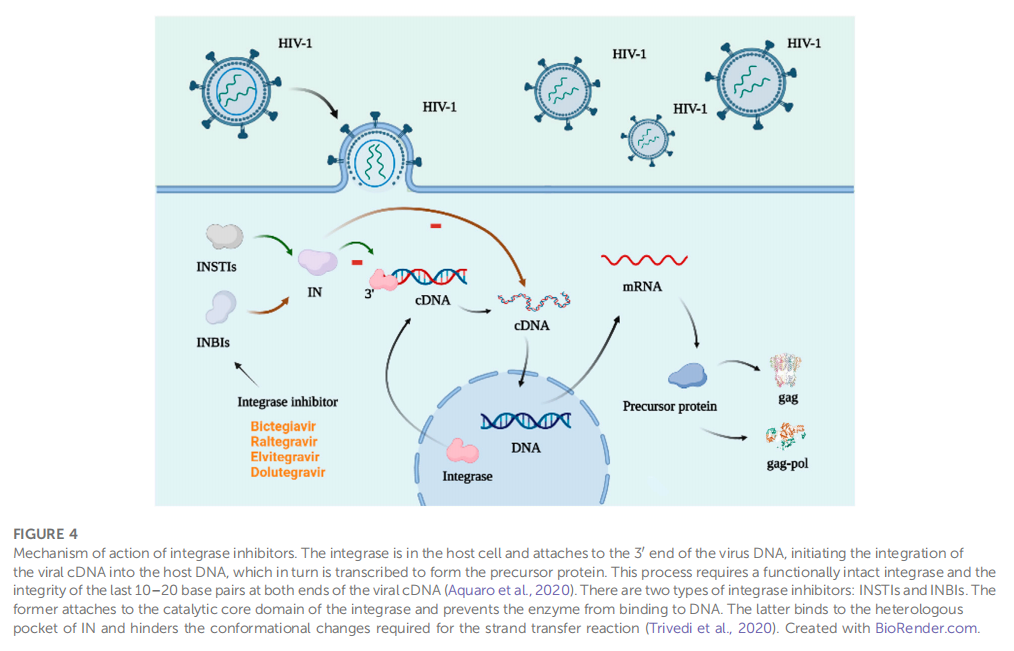
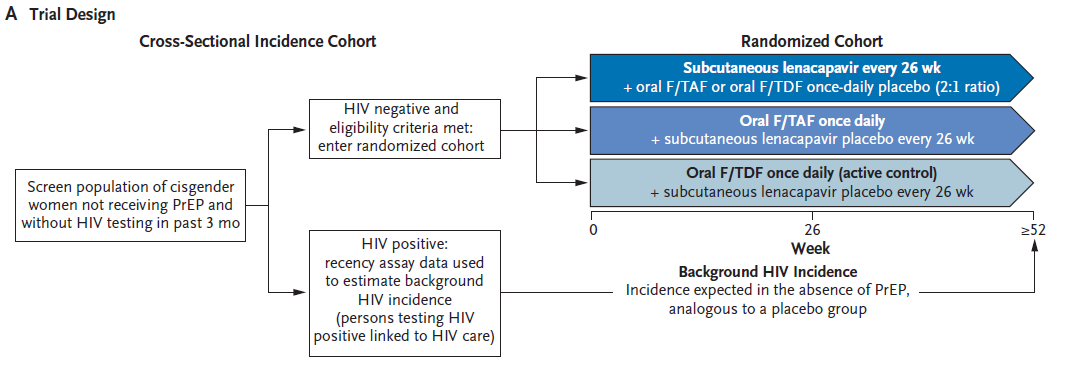
2021年12月3日,吉利德HIV新药三合一复方片剂必妥维®(比克恩丙诺片)首次进入2021版国家医保目录。2020年1月1日吉利德在北京宣布必妥维®正式在中国上市。也就是说,这距离必妥维在中国正式上市仅仅不到两年的时间,国家医保局就火速批准了该药纳入医保支付范围,目的是让临床价值高的抗病毒新药惠及更多的HIV感染者。 “防治艾滋病具有明显临床优势”,使得必妥维®优先审批、快速进医保2018年2月,美国FDA率先批准吉利德HIV新药必妥维®在美国上市,4个月后,必妥维®顺利在欧盟获批。仅仅一年多的时间,2019年8月我国批准必妥维®在华上市,在2020年的元旦当天,吉利德在北京召开新闻发布会,正式宣布必妥维®在中国上市。2021年12月3日,国家医保局又带给我们带来一个好消息,吉利德抗HIV新药必妥维®进入2021版国家医保目录。从获批到上市,再从上市到进医保,必妥维®在中国仅用了短短两年的时间。这得益于国家药品监督管理局(NMPA)和国家医保局优先审批的政策,对防治艾滋病具有明显优势的药物可以优先审批审评,进一步提高创新药物的可及性,惠及广大HIV感染者。
“防治艾滋病具有明显临床优势”,使得必妥维®优先审批、快速进医保2018年2月,美国FDA率先批准吉利德HIV新药必妥维®在美国上市,4个月后,必妥维®顺利在欧盟获批。仅仅一年多的时间,2019年8月我国批准必妥维®在华上市,在2020年的元旦当天,吉利德在北京召开新闻发布会,正式宣布必妥维®在中国上市。2021年12月3日,国家医保局又带给我们带来一个好消息,吉利德抗HIV新药必妥维®进入2021版国家医保目录。从获批到上市,再从上市到进医保,必妥维®在中国仅用了短短两年的时间。这得益于国家药品监督管理局(NMPA)和国家医保局优先审批的政策,对防治艾滋病具有明显优势的药物可以优先审批审评,进一步提高创新药物的可及性,惠及广大HIV感染者。
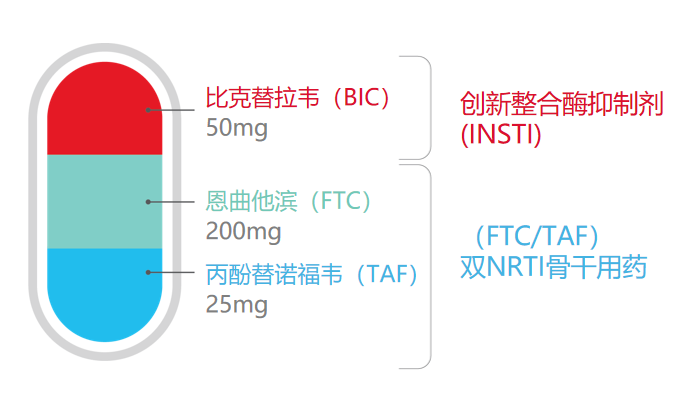 必妥维®组成结构示意图
必妥维®组成结构示意图
国家药品监督管理总局(NMPA)对必妥维®的审批是基于4项III期临床研究的数据,4项研究共纳入2414名初治和病毒学抑制的经治HIV成人感染者,结果发现,在48周时,受试者均达到了非劣效性的主要病毒学终点指标,在第96周时,必妥维®的病毒学抑制率高达99.8%。值得一提的是,必妥维®组在治疗期间没有一位参与者发生病毒学耐药,也没有任何参与者因肾脏、骨骼或肝脏不良事件而停药。单片复方制剂提高了服药的依从性,满足了临床上对HIV感染者治疗的更高需求。据悉,必妥维®(比克替拉韦50mg /恩曲他滨200mg/丙酚替诺福韦25mg,BIC/FTC/TAF)是目前基于整合酶抑制剂的最小三合一单片复方制剂,具有快速、高效、持久抑制HIV的特点,为HIV感染者带来了新的治疗选择。作为最新型的三合一复方制剂,必妥维®采用了具有更高病毒学抑制靶点的整合酶抑制剂比克替拉韦(BIC)和对肾脏、骨骼安全性更高的替诺福韦前体药物丙酚替诺福韦(TAF),概括起来具有以下优势: 方便:不需要检测超敏因子HLA-B 5701,不受基线耐药结果、病毒载量和CD4计数限制;全面:全面覆盖轻中度肾功能不全的患者、面临骨质疏松风险的老年患者;简单:目前最小的三联单片复方制剂,无需随餐,依从性更好。
一天一片,强效安全,必妥维®是HIV感染者终身服药的新选择
近10年来,我国艾滋病的防控工作取得了巨大成就,HIV病毒感染始终控制在低流行水平,临床诊治水平不断延长,尤其是抗病毒药物的使用让HIV的寿命得到明显延长。HIV感染一旦确诊需终身服药,对于需要持续的抑制病毒外,长期用药的安全性、简便性以及可负担性成为新的要求。必妥维®是全球权威指南一致推荐的HIV初治首选方案,服用方便,一天一片,不受食物同服限制,药物相互作用少,给HIV感染者带来了更为高效便捷的用药选择。随着必妥维®进入2021年版的国家医保目录,相信会有更多的HIV感染者选择使用新的药物,进一步提高临床效果,减少长期服药的副作用,早日达到三个90%的艾滋病防治目标(艾滋病发现率90%、抗病毒治疗率90%和治疗有效率90%)。  健客医生官方号
健客医生官方号
 必妥维®组成结构示意图
必妥维®组成结构示意图