Nature Medicine|乌司奴单抗对1型糖尿病的影响超预期!临床试验首次揭示TH17细胞的新角色
 学术前沿官方号
学术前沿官方号1型糖尿病(T1D)是一种由免疫系统攻击胰岛β细胞引发的自身免疫性疾病,导致胰岛素分泌不足。目前,尽管已经有多个自身免疫性疾病成功应用免疫调节疗法,T1D的主要治疗手段仍是胰岛素替代,但这并未能在所有患者中实现理想的血糖控制,尤其是对于青少年患者。
保护残余的内源性胰岛素分泌能力有助于减少短期和长期的并发症,为此,针对T1D致病机制中的免疫途径成为治疗的关键方向。乌司奴单抗(Ustekinumab)作为一种针对IL-12和IL-23的单克隆抗体,可通过抑制TH17.1细胞的功能,展现出延缓β细胞功能丧失的潜力。最近,Nature Medicine上发表了一项多中心、双盲、随机对照的二期临床试验结果,探讨了乌司奴单抗在青少年T1D中的应用潜力,为T1D治疗提供了一条全新的免疫调节途径。这一发现不仅为青少年T1D患者带来了新的希望,也为未来大规模临床应用奠定了基础。
研究方法
该研究为一项多中心、双盲、随机的Ⅱ期临床试验,旨在评估乌司奴单抗对青少年1型糖尿病(T1D)患者的疗效和安全性。研究在多个中心进行,时间从2018年12月至2022年9月,包括疫情期间。研究共筛选出262名符合条件的患者,最终纳入了72名12-18岁的近期诊断为T1D的青少年,按照2:1的比例随机分配到乌司奴单抗治疗组(n=41)和安慰剂组(n=21)。纳入标准包括β细胞自身抗体阳性,排除标准包括β细胞自身抗体阴性、无法完成混合膳食耐受试验(MMTT)、结核测试阳性或COVID相关问题等。主要终点为治疗12个月后的β细胞功能(通过测量C肽),次要结局包括治疗组患者的TH17.1细胞减少情况等。
研究结果
主要结果
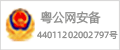
● C肽AUC:研究的主要结果评估在52周时得出。结果显示,乌司奴单抗在52周时与安慰剂组相比,C肽AUC增加了49%(乌司奴单抗组为0.45 nmol l−1 min−1,安慰剂组为0.30 nmol l−1 min−1,几何比=1.49;P = 0.02)。
● 效果延迟:尽管药物水平持续存在,乌司奴单抗的效果在前28周延迟出现,在此期间,两组的C肽AUC下降幅度相似(乌司奴单抗组为0.49 nmol l−1 min−1,安慰剂组为0.42 nmol l−1 min−1,几何比=1.15;P = 0.45)。
 主要代谢结果指标
主要代谢结果指标
a) 52周内干预组(乌司奴单抗组)与对照组(安慰剂组)的几何比值(及95%置信区间)
b) 根据治疗组调整后的C肽AUC(nmol l⁻¹ min⁻¹)在52周内的变化
红色表示乌司奴单抗组,蓝色表示安慰剂组
次要结果
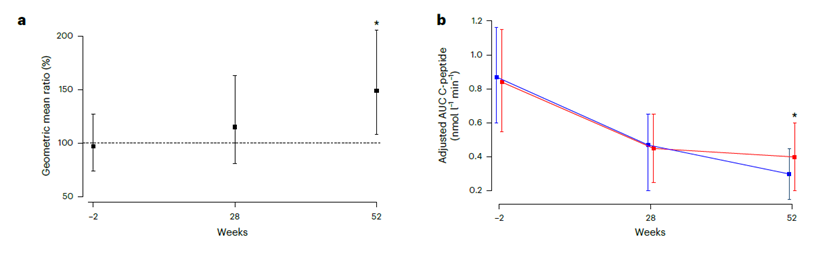
● HbA1c水平:两组HbA1c水平从基线的50 mmol/mol上升到52周的56 mmol/mol,组间无差异(乌司奴单抗与安慰剂在52周时的平均差异=-0.83,95%CI:-7.2-5.55,P=0.15)。
● 外源性胰岛素使用:两组从基线到52周的外源性胰岛素使用均增加,但调整基线因素后,组间无差异(平均差异=0.04,95%CI:-0.13-0.21,P=0.38)。
● 胰岛素剂量调整后的HbA1c(IDAA1c):两组IDAA1c均增加,但组间无差异(平均差异=0.23,95%CI:-0.79-1.24,P=0.65)。
 次要代谢结果指标
次要代谢结果指标
c) HbA1c(mmol/mol)在52周内的变化
d) 调整体重后的每日外源性胰岛素使用量在52周内的变化
e) IDAA1c在52周内的变化
红色表示乌司奴单抗组,蓝色表示安慰剂组
安全性和药物水平
● 耐受性:乌司奴单抗耐受性良好,无与治疗相关的严重不良事件。
● 药物水平:除1名在28周的受试者外,所有接受活性药物的受试者在研究期间乌司奴单抗水平均高于0.8 μg/ml的治疗水平。
探索性结果
● 细胞因子产生:尽管乌司奴单抗组中产生IFNγ的CD4 T细胞频率未减少,但产生IL-17A的TH17细胞和同时产生IL-17A与IFNγ的TH17.1细胞频率显著减少(TH17.1细胞减少在28周时显现,TH17和TH17.1细胞在52周时显现)
● 免疫反应:TH17.1细胞同时分泌GM-CSF和/或IL-2的亚群减少最为显著,在治疗开始的12周就显示出小幅减少,在28和52周时显著减少(P < 0.001)。其他细胞亚群的数量和频率如T细胞、CD4 T细胞、CD8 T细胞及自然杀伤细胞(NK细胞)等未出现与治疗相关的显著变化。
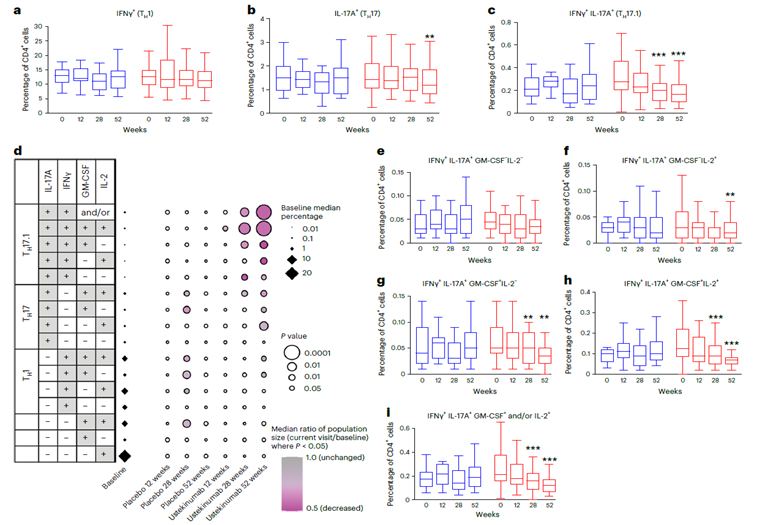 分析接受乌司奴单抗和安慰剂治疗的个体中细胞因子产生CD4 T细胞亚群的频率
分析接受乌司奴单抗和安慰剂治疗的个体中细胞因子产生CD4 T细胞亚群的频率
a–c) 显示产生IFNγ(a; TH1细胞)、IL-17A(b; TH17细胞)以及IFNγ和IL-17A(c; TH17.1细胞)的CD4+ T细胞频率的箱线图(第28周,P = 0.001;第52周,P < 0.0001)。
d) 显示治疗期间细胞因子产生CD4 T细胞亚群变化的点图
e–i) 不同细胞因子组合中CD4+ T细胞频率的箱线图
红色表示乌司奴单抗组,蓝色表示安慰剂组
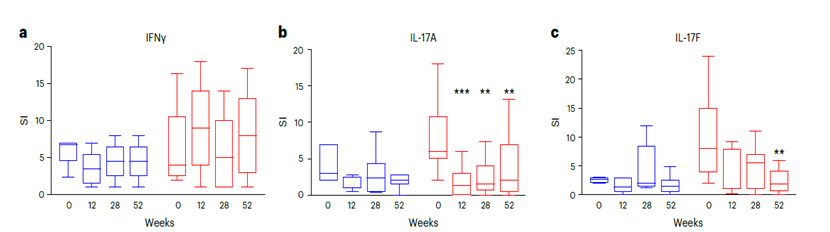 在接受乌司奴单抗和安慰剂治疗的个体中,对胰岛素原刺激产生IL-17A的细胞的箱线图
在接受乌司奴单抗和安慰剂治疗的个体中,对胰岛素原刺激产生IL-17A的细胞的箱线图
a) IFNγ响应
b) IL-17A响应(第12周,P = 0.0003;第28周,P = 0.006;第52周,P = 0.002)
c) IL-17F响应(第52周,P = 0.002)
SI为胰岛素原刺激孔中的平均斑点数/未刺激孔中的平均斑点数。基线SI < 2的个体被移除。
事后分析
● C肽水平与免疫反应的关系:乌司奴单抗组中,表现出细胞因子分泌细胞减少更多的受试者(即“高免疫反应者”)C肽保留更好。具体而言,与随机分配到安慰剂组的参与者相比,分配到乌司奴单抗组的参与者在28到52周内C肽水平保持稳定的几率(OR)为3.81(95% CI:1.10-13.2,P = 0.03)。在TH17.1细胞减少最明显的参与者中,OR增加到8.80(95% CI:1.46-52.8,P = 0.01),而安慰剂组未观察到显著关联(OR = 1.67,95% CI:0.13-20.6,P = 0.69)。
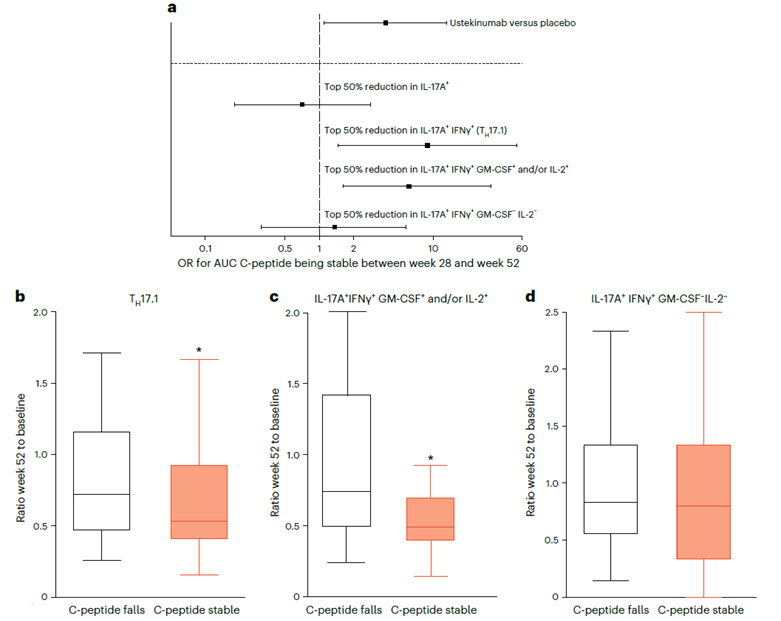 免疫参数变化与主要代谢结果之间的关系
免疫参数变化与主要代谢结果之间的关系
a) 28至52周期间C肽水平稳定或增加的几率比(OR)及其95%置信区间(CI)
b–d) 28至52周期间C肽稳定性分层的免疫群体变化(以第52周相对于基线的频率比表示)的箱线图
b) TH17.1细胞在第52周相对于基线的变化(P = 0.03)
c) IL-17A+IFNγ+GM-CSF+和/或IL-2+在第52周相对于基线的变化(P = 0.02)
d) IL-17A+IFNγ+GM-CSF−IL-2−在第52周相对于基线的变化
敏感性分析
● 为验证主要结果的稳健性,进行了敏感性分析。排除了偶然揭盲的参与者、主要结果访视延迟6个月的参与者和具有遗传性红细胞疾病影响HbA1c的参与者后,主要结果无变化,表明分析模型对少数协议偏差和极端值具有稳健性。
总 结
本研究的主要结论是乌司奴单抗通过靶向IL-12/IL-23通路,在新诊断的1型糖尿病(T1D)儿童和青少年中表现出较高的安全性,并有效保护β细胞功能。重要的是,研究首次为TH17细胞在T1D中的致病作用提供了前瞻性随机对照试验的证据,证实了之前初步研究的数据。
探究性机制数据表明,一小部分TH17细胞与β细胞功能丧失密切相关,乌司奴单抗可减少该细胞群体,进而维持C肽水平。该研究还发现,乌司奴单抗对免疫系统的影响较为选择性,从而表现出良好的不良事件安全性。此外,该药物的治疗效果具有延迟性,通常需要6到12个月才能显现。虽然该研究未能显著改善其他代谢参数,但其结果为进一步研究乌司奴单抗在T1D早期阶段的预防作用提供了依据。
然而,该研究也存在一些局限性,包括T细胞检测作为探索性终点而非主要终点,且未对多重检验进行调整。此外,研究未能检测到代谢参数变化,这可能是由于样本量不足以及药物作用的延迟性。尽管如此,研究结果为未来在更早期疾病阶段使用乌司奴单抗或类似药物提供了理论依据,可能有助于延缓或减少T1D患者对胰岛素的需求。
对于临床医生来说,这项研究的意义在于确认了乌司奴单抗在T1D治疗中的潜在作用,尤其是在β细胞保护方面,为开发新的治疗策略提供了方向。同时,它也提示了在T1D治疗中可能需要更早期干预,并考虑使用具有不同作用机制的生物制剂。未来的研究需要进一步验证这些发现,并探索最佳的治疗时机和药物组合,以实现对T1D更有效的管理。
参考文献:
Tatovic D, Marwaha A, Taylor P et al. Ustekinumab for type 1 diabetes in adolescents: a multicenter, double-blind, randomized phase 2 trial. Nat Med. 2024 Jul 30. doi: 10.1038/s41591-024-03115-2.
原创文章:方舟健客版权所有,未经许可不得转载。