本周「12.27-1.3」资讯:新年开局重磅!吉利德长效抗HIV药物国内获批|礼来替尔泊肽在国内上市|月度FDA批准药品信息汇总
 医周动态官方号
医周动态官方号一、告别繁琐用药!吉利德一年两次的长效抗HIV药物在国内获批
图源:https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250102154109161.html
本周(1月2日),吉利德科学(Gilead Sciences)的长效抗人类免疫缺陷病毒(HIV)药物——来那帕韦片与来那帕韦注射液(英文名:Lenacapavir),已成功获得中国国家药监局(NMPA)官网批准上市,用于与其他抗反转录病毒药物联合使用,治疗当前方案无法达到病毒学抑制的多重耐药1型HIV(HIV-1)感染的成人患者。
来那帕韦注射液是第一种每年用药两次的长效注射治疗HIV的药物,也是全球首个获批的衣壳抑制剂,主要通过干扰病毒生命周期的多个基本步骤来抑制HIV-1复制,包括衣壳介导的HIV-1前病毒DNA的核摄取(通过阻断核输入蛋白与衣壳的结合),病毒的组装和释放(通过干扰Gag/Gag-pol功能,减少衣壳蛋白亚基的产生),以及衣壳核的形成(通过破坏衣壳亚基结合的速率,导致衣壳畸形)。

图源:https://mp.weixin.qq.com/s/ceVvpite5yfU_ueW4_HJyQ
在此前的国际艾滋病大会上,来那帕韦用于预防HIV的一项三期、双盲、随机、对照试验PURPOSE 1惊艳发布,该研究近期也发表在了《新英格兰医学杂志》(NEJM)上,研究结果显示,一年两次注射来那卡帕韦,在减少HIV发病率方面显示出100%的有效性,实现零HIV新发病例,是 HIV预防的重大革新。
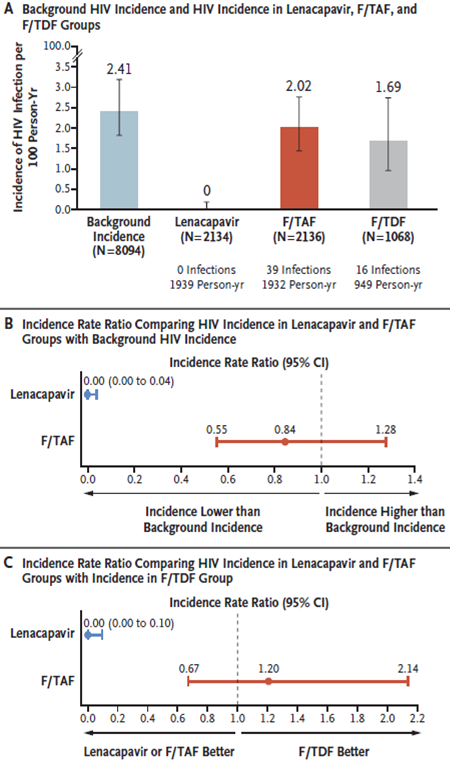
PURPOSE 1:HIV发病率汇总
与既往的需要每日口服的HIV暴露前预防(PrEP)药物相比,长效抗HIV药物优势显著,不仅可以降低给药频率,减少每日用药的心理负担,更大程度上保护了HIV感染者的疾病隐私,而且DDI少,有助于提高其用药依从性和生活质量。
目前,已经在国内外上市的长效药物有:卡替拉韦(Cabotegravir,CAB)+利匹韦林(Rilpivirine,RPV)注射剂、注射用艾博韦泰(Albuvirtide,ABT)、来那帕韦注射液、伊巴珠单抗(Ibalizumab,IBA)注射剂。既往在我国获批的两款长效抗HIV药物分别是CAB+RPV注射剂和ABT注射剂,此次来那帕韦在我国的获批上市,为国内的HIV患者带来了新的治疗选择和希望。
二、礼来替尔泊肽中国登场,降糖减重双优,头对头击败司美格鲁肽
本周(1月2日),礼来(Lilly)中国重磅宣布,穆峰达®(替尔泊肽注射液)正式在中国上市,标志着这款全球首个GIP/GLP-1双受体激动剂的药物在中国市场的正式亮相。

图源:https://mp.weixin.qq.com/s/P89fmriiGjEfY_yvB3Z8rg
替尔泊肽的上市同时覆盖了两大适应症:成人2型糖尿病(T2DM)患者的血糖控制不佳的治疗,以及肥胖/超重成人的长期体重管理。这两类适应症分别于2024年5月和7月获得国家药品监督管理局批准,目前在中国上市的4种规格为:2.5mg: 0.5ml,5mg: 0.5ml,7.5mg: 0.5ml,10mg: 0.5ml。
在T2DM治疗领域,针对饮食和运动配合二甲双胍和/或磺脲类药物仍控糖不佳的成人患者,替尔泊肽表现卓越。临床研究表明,其10mg治疗组患者经 40 周治疗,血糖(HbA1c)平均降幅达2.37%,高达89%的患者实现 HbA1c达标(<7%),同时体重平均降低10.3公斤。在二甲双胍治疗不佳的T2DM患者中,加用替尔泊肽10mg治疗52周后,葡萄糖目标范围内时间(TIR)可达93%,有力证明其平稳控糖能力。
在体重管理方面,对于初始体重指数(BMI)≥28kg/m²(肥胖)或≥24kg/m²(超重)且伴有至少一种体重相关合并症的成人,替尔泊肽效果显著。在 72 周治疗中,10mg治疗组患者平均体重最高降幅达 21.4%,腰围平均下降 19.4cm,是首个3期研究中让肥胖/超重患者平均减重超20%的药物。
尤为引人注目的是,在全球范围内进行的头对头3b期临床试验SURMOUNT-5结果显示,在肥胖或伴有体重相关合并症的非糖尿病超重成人中,治疗72周后,替尔泊肽减重效果(平均减重20.2%)大幅优于司美格鲁肽(平均减重13.7%),替尔泊肽组相对体重减轻是司美格鲁肽组的 1.47 倍,在多个关键次要终点上也全面领先。且替尔泊肽在中国人群为主的亚太地区患者中总体安全性良好,胃肠道反应常见但多为轻中度且随时间缓解。
礼来替尔泊肽的上市无疑为中国肥胖及T2DM患者带来了新的治疗选择,尤其对于控制体重困难的超重患者,提供了有效的解决方案,未来有望成为治疗肥胖及糖尿病的标准疗法之一。
三、FDA十二月份批准药品信息汇总
以下是2024年12月FDA批准的药物及新适应症汇总,涵盖了多种癌症、血友病、囊性纤维化等疾病的治疗药物,这些药物为相关患者群体提供了新的治疗选择。
1. Bizengri(zenocutuzumab-zbco)注射液
• 公司:Merus公司
• 批准日期:2024年12月4日
• 适应症:NRG1融合阳性的非小细胞肺癌和胰腺癌
• 药物信息:Bizengri是一种双特异性HER2和HER3抗体,用于治疗NRG1融合阳性的非小细胞肺癌和胰腺癌。
2. Unloxcyt(cosibelimab-ipdl)注射液
• 公司:Checkpoint Therapeutics公司
• 批准日期:2024年12月13日
• 适应症:皮肤鳞状细胞癌
• 药物信息:Unloxcyt是一种PD-L1阻断抗体,用于治疗皮肤鳞状细胞癌。
3. Crenessity(crinecerfont)胶囊和口服溶液
• 公司:Neurocrine Biosciences公司
• 批准日期:2024年12月13日
• 适应症:经典型先天性肾上腺增生症
• 药物信息:Crenessity是一种促肾上腺皮质激素释放因子1型受体拮抗剂,用于与糖皮质激素替代治疗联合控制成人和儿童经典型先天性肾上腺增生症中的雄激素水平。
4. Steqeyma(ustekinumab-stba)注射液
• 公司:Celltrion USA
• 批准日期:2024年12月17日
• 适应症:斑块型银屑病、银屑病关节炎、克罗恩病、溃疡性结肠炎
• 药物信息:Steqeyma是一种人类白介素12和23拮抗剂,为Stelara的生物类似药,用于治疗多种免疫介导的疾病。
5. Ensacove(ensartinib)胶囊
• 公司:Xcovery控股公司(Xcovery Holdings, Inc.)
• 批准日期:2024年12月18日
• 适应症:ALK阳性非小细胞肺癌
• 药物信息:Ensacove是一种间变性淋巴瘤激酶(ALK)抑制剂,用于治疗ALK阳性局部晚期或转移性非小细胞肺癌。
6. Ryoncil(remestemcel-L-rknd)静脉输注细胞悬液
• 公司:Mesoblast公司
• 批准日期:2024年12月18日
• 适应症:类固醇耐药急性移植物抗宿主病
• 药物信息:Ryoncil是一种同种异体骨髓来源的间充质干细胞疗法,用于治疗2个月及以上儿童患者的类固醇难治性急性移植物抗宿主病。
7. Symvess(无细胞组织工程血管-tyod)用于外科血管移植
• 公司:Humacyte公司
• 批准日期:2024年12月19日
• 适应症:血管重建手术
• 药物信息:Symvess是一种首创的无细胞生物工程化人类组织,用于治疗四肢血管创伤。
8. Tryngolza(olezarsen)注射液
• 公司:Ionis制药公司(Ionis Pharmaceuticals, Inc.)
• 批准日期:2024年12月19日
• 适应症:家族性乳糜微粒血症
• 药物信息:Tryngolza是一种靶向apoC-III的反义寡核苷酸,作为饮食辅助手段用于降低成人家族性乳糜微粒血症患者的甘油三酯水平。
9. Alyftrek(deutivacaftor、tezacaftor 和 vanzacaftor)
• 公司:Vertex制药公司(Vertex Pharmaceuticals Incorporated)
• 批准日期:2024年12月20日
• 适应症:囊性纤维化
• 药物信息:Alyftrek是一种新一代三联囊性纤维化跨膜传导调节因子(CFTR)调节剂,用于治疗囊性纤维化。
10. Alhemo(concizumab-mtci)注射液
• 公司:诺和诺德(Novo Nordisk)
• 批准日期:2024年12月20日
• 适应症:伴有抑制剂的A型血友病和B型血友病
• 药物信息:Alhemo是一种组织因子途径抑制剂(TFPI)拮抗剂,用于血友病A和B患者的常规预防,减少出血事件的发生。
11. Opdivo Qvantig(nivolumab 和 hyaluronidase-nvhy)皮下注射液
• 公司:百时美施贵宝(Bristol-Myers Squibb)
• 批准日期:2024年12月27日
• 适应症:肾细胞癌、黑色素瘤、非小细胞肺癌、头颈部鳞状细胞癌、尿路上皮癌、结直肠癌、肝细胞癌、食管癌、胃癌、胃食管交界癌和食管腺癌
• 药物信息:Opdivo Qvantig是一个PD-1受体阻断抗体和透明质酸酶的组合,用于治疗多种实体瘤。
参考:
1. 国家药品监督管理局. 2025年01月02日药品批准证明文件送达信息. Available from: https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250102154109161.html
2. Bekker LG, Das M, Abdool Karim Q, et al. Twice-Yearly Lenacapavir or Daily F/TAF for HIV Prevention in Cisgender Women. N Engl J Med. 2024 Jul 24. doi: 10.1056/NEJMoa2407001.
3. Gilead Sciences . 每年两次给药的HIV长效疗法萨兰卡®在华获批. 2025年01月02日. Available from: https://mp.weixin.qq.com/s/ceVvpite5yfU_ueW4_HJyQ
4. 李凌华,蔡琳,陈雅红,等.长效抗HIV药物临床应用专家共识.中国艾滋病性病,2024,30(12):1230-1239.
5. 礼来Lilly. 礼来穆峰达®(替尔泊肽)在华上市!Available from: https://mp.weixin.qq.com/s/P89fmriiGjEfY_yvB3Z8rg
6. 礼来Lilly. 头对头研究显示礼来替尔泊肽减重效果优于司美格鲁肽. Available from: https://mp.weixin.qq.com/s/KbDkJ7a32XdEmLDTdYn7iQ
7. ClinicalTrials.gov. A Study of Tirzepatide (LY3298176) in Participants With Obesity or Overweight With Weight Related Comorbidities (SURMOUNT-5). Last Update Posted: 2024-12-11. Available from: https://clinicaltrials.gov/study/NCT05822830
8. Drugs.com. New Drug Approvals. Available from: https://www.drugs.com/newdrugs.html
9. Drug Approvals and Databases. FDA. Available from: https://www.fda.gov/drugs/development-approval-process-drugs/drug-approvals-and-databases
原创文章:方舟健客版权所有,未经许可不得转载。